题目内容
4.某温度下,在2L的密闭容器中,加入1mol X(g)和2mol Y(g)发生反应:X(g)+mY(g)?3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变,下列叙述不正确的是( )| A. | m=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | X与Y平衡转化率之比为1:1 | |
| D. | 第二次平衡时,Z的浓度为0.4mol•L-1 |
分析 向平衡体系中再加入1molZ,重新建立平衡时X、Y、Z的体积分数不变,说明压强不影响该平衡,则反应前后总计量数相等,则1+m=3,m=2;X、Y的初始浓度之比为1:2,计量数之比为1:2,则二者的转化率相等;根据重新达到平衡时Z的体积分数不变及反应过程中总物质的量不变计算出Z的物质的量,再根据c=$\frac{n}{V}$计算出Z的浓度;平衡常数的影响因素是温度.
解答 解:A.向平衡体系中再加入1molZ,重新建立平衡时X、Y、Z的体积分数不变,说明压强不影响该平衡,则反应前后总计量数相等,则1+m=3,m=2,故A正确;
B.同一化学反应的平衡常数只与温度有关,两次平衡时温度不变,故两次平衡的平衡常数相同,故B正确;
C.向2L的密闭容器中加入1molX和2molY,由于m=2,则反应过程中消耗X、Y的物质的量之比为1:2,所以X、Y的转化率一定相等,即X与Y平衡转化率之比为1:1,故C正确;
D.再加入1molZ后总物质的量为4mol,重新达到平衡时Z的体积分数仍然为10%,则重新建立平衡时Z的浓度为:$\frac{4mol×10%}{2L}$=0.2mol/L,故D错误;
故选D.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学平衡及其影响因素为解答关键,注意掌握化学平衡常数的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
14.碱式碳酸铜Cu2(OH)2CO3又称为铜绿,属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
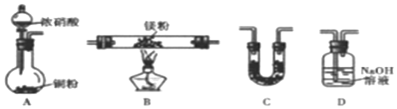
12.完成下列实验所需选择的装置或仪器都正确的是( )
| A | B | C | D | |
| 实验 | 分离汽油和水 | 通过蒸馏乙醇的水溶 液获得无水乙醇 | 分离 CCl4 中的 I2 | 除去 CO2 气体中的 HCl 气体 |
| 装 置 或 仪 器 | 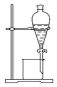 | 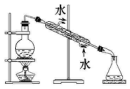 | 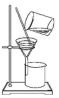 | 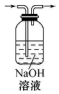 |
| A. | A | B. | B | C. | C | D. | D |
16.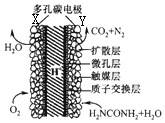 直接尿素电池的结构如图所示,下列说法不正确的是( )
直接尿素电池的结构如图所示,下列说法不正确的是( )
 直接尿素电池的结构如图所示,下列说法不正确的是( )
直接尿素电池的结构如图所示,下列说法不正确的是( )| A. | 电池工作时,化学能转化为电能 | |
| B. | 电池工作时,H+向Y极区迁移,Y极周围溶液的pH减小 | |
| C. | 碳电池采用多孔并用触媒层可加快反应速率 | |
| D. | Y极的电极反应式为H2NCONH2+H2O-6e-═N2↑+CO2+6H+ |
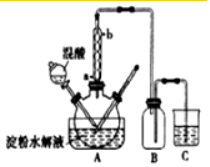
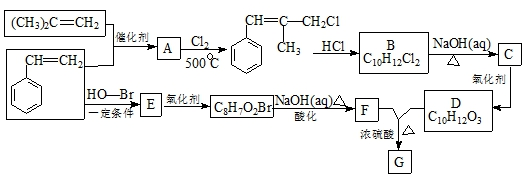
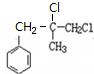 ,B生成C的反应类型为取代反应;
,B生成C的反应类型为取代反应;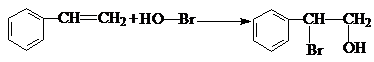 .
.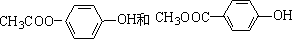 .
. ) 的合成线路:
) 的合成线路: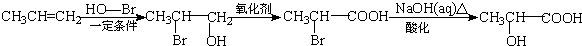 .
.