题目内容
(1)已知石棉是硅酸盐矿物,某种石棉的化学式可表示为Ca2Mg5Si8O22(OH)2,将其改写成氧化物的形式 .
(2)Na2SiO3易溶于水,水溶液称“ ”,是建筑行业的黏合剂,也用于木材的防腐和防火.写出二氧化硅与烧碱反应得到Na2SiO3的离子方程式: ;
(3)根据铝与强碱反应的化学方程式回答下列相关问题:Al+2NaOH+2H2O═2NaAlO2+3H2↑
(4)该反应中,氧化剂是 ,还原剂是 ;
(5)若反应消耗0.1mol Al,则生成气体的体积是 ;
(6)该反应的离子方程式是 .
(2)Na2SiO3易溶于水,水溶液称“
(3)根据铝与强碱反应的化学方程式回答下列相关问题:Al+2NaOH+2H2O═2NaAlO2+3H2↑
(4)该反应中,氧化剂是
(5)若反应消耗0.1mol Al,则生成气体的体积是
(6)该反应的离子方程式是
考点:含硅矿物及材料的应用,氧化还原反应
专题:氧化还原反应专题,碳族元素
分析:(1)硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO?nSiO2?mH2O);
(2)二氧化硅能与氢氧化钠反应生成硅酸钠和水;
(3)金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O=2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH=NaAlO2+2H2O
(4)根据化合价的变化分析;
(5)根据方程式计算;
(6)根据化学方程式写出离子方程式.
(2)二氧化硅能与氢氧化钠反应生成硅酸钠和水;
(3)金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O=2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH=NaAlO2+2H2O
(4)根据化合价的变化分析;
(5)根据方程式计算;
(6)根据化学方程式写出离子方程式.
解答:
解:(1)硅酸盐改写成氧化物形式时:活泼的金属氧化物写在前面,再写SiO2,含有氢元素的H2O最后写,Ca2Mg5Si8O22(OH)2可表示为:2CaO?5MgO?8SiO2?H2O,
故答案为:2CaO?5MgO?8SiO2?H2O;
(2)二氧化硅能与氢氧化钠反应生成硅酸钠和水,反应的化学方程式为:SiO2+2NaOH═Na2SiO3+H20,离子方程式:SiO2+2OH-=SiO32-+H2O;
故答案为:SiO2+2OH-=SiO32-+H2O;
(3)金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O=2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH=NaAlO2+2H2O
(4)反应中Al的化合价升高,作还原剂,水中H元素的化合价降低,水作氧化剂,故答案为:H2O;Al;
(5)已知2Al+2NaOH+2H2O═2NaAlO2+3H2↑,则反应消耗0.1mol Al,则生成气体为0.15mol,其体积是3.36L;故答案为:3.36L;
(6)已知2Al+2NaOH+2H2O═2NaAlO2+3H2↑,则离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑.
故答案为:2CaO?5MgO?8SiO2?H2O;
(2)二氧化硅能与氢氧化钠反应生成硅酸钠和水,反应的化学方程式为:SiO2+2NaOH═Na2SiO3+H20,离子方程式:SiO2+2OH-=SiO32-+H2O;
故答案为:SiO2+2OH-=SiO32-+H2O;
(3)金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O=2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH=NaAlO2+2H2O
(4)反应中Al的化合价升高,作还原剂,水中H元素的化合价降低,水作氧化剂,故答案为:H2O;Al;
(5)已知2Al+2NaOH+2H2O═2NaAlO2+3H2↑,则反应消耗0.1mol Al,则生成气体为0.15mol,其体积是3.36L;故答案为:3.36L;
(6)已知2Al+2NaOH+2H2O═2NaAlO2+3H2↑,则离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑;
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑.
点评:本题考查了硅酸盐、二氧化硅、Al的性质等,涉及氧化还原反应、离子方程的书写,题目难度中等,注意金属铝与氢氧化钠溶液反应的实质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列对于苯的叙述正确的是( )
| A、易被强氧化剂KMnO4等氧化 |
| B、属于不饱和烃易发生加成反应 |
| C、属于不饱和烃但比较易发生取代反应 |
| D、苯是一种重要的有机溶剂可广泛应用于生产绿色油漆等 |
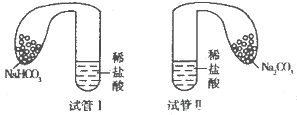
 甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体.X、Y是化合物.X溶液呈淡绿色.它们之间有如图1所示转化关系.
甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体.X、Y是化合物.X溶液呈淡绿色.它们之间有如图1所示转化关系.