题目内容
下列结论正确的是( )
①离子的还原性:S2->Cl->Br->I-
②酸性:H2SO4>H3PO4>H2CO3>HClO
③微粒半径:K+>Al3+>S2->Cl-
④氢化物的稳定性:HF>HCl>H2S>PH3.
①离子的还原性:S2->Cl->Br->I-
②酸性:H2SO4>H3PO4>H2CO3>HClO
③微粒半径:K+>Al3+>S2->Cl-
④氢化物的稳定性:HF>HCl>H2S>PH3.
| A、①③ | B、只有① | C、①④ | D、②④ |
分析:①元素的非金属性越强,对应阴离子的还原性越弱;
②元素的非金属性越强,最高价氧化物对应的水化物的酸性越强;
③核外电子排布相同的离子,核电核数越大,半径越小;离子的原子核外电子层数越多,半径越大;
④元素的非金属性越强,氢化物越稳定;
②元素的非金属性越强,最高价氧化物对应的水化物的酸性越强;
③核外电子排布相同的离子,核电核数越大,半径越小;离子的原子核外电子层数越多,半径越大;
④元素的非金属性越强,氢化物越稳定;
解答:解:①非金属性:Cl>Br>I>S,非金属性越强,对应阴离子的还原性越弱,还原性为:S2->I->Br->Cl-,故①错误;
②非金属性:S>P>C,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,又H2CO3酸性大于HClO,所以酸性:H2SO4>H3PO4>H2CO3>HClO,故②正确;
③K+、S2-、Cl-原子核外电子排布相同,核外电子排布相同的离子,核电核数越大,半径越小,离子的原子核外电子层数越多,所以半径::S2->Cl->K+>Al3+,故③错误;
④非金属性:F>Cl>S>P,元素的非金属性越强,氢化物越稳定,所以稳定性:HF>HCl>H2S>PH3,故④正确;
故选:D;
②非金属性:S>P>C,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,又H2CO3酸性大于HClO,所以酸性:H2SO4>H3PO4>H2CO3>HClO,故②正确;
③K+、S2-、Cl-原子核外电子排布相同,核外电子排布相同的离子,核电核数越大,半径越小,离子的原子核外电子层数越多,所以半径::S2->Cl->K+>Al3+,故③错误;
④非金属性:F>Cl>S>P,元素的非金属性越强,氢化物越稳定,所以稳定性:HF>HCl>H2S>PH3,故④正确;
故选:D;
点评:本题考查元素周期表与周期律的递变性,明确同周期、同主族元素的性质变化规律及元素非金属性的比较方法是解答本题的关键,难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
己知:2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
| A、H2的燃烧热△H=-241.8kJ?mol-1 | B、炭和和水蒸气转化为水煤气为放热反应 | C、将24g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0kJ?mol-1 | D、1mol H2O(g)完全分解需要吸收241.8kJ热量 |
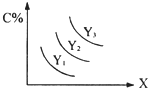 对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )
对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )| A、Y表示温度,X表示压强,且Y3>Y2>Y1 | B、Y表示压强,X表示温度,且Y3>Y2>Y1 | C、X表示压强,Y表示温度,且Y1>Y2>Y3 | D、X表示温度,Y表示压强,且Y1>Y2>Y3 |