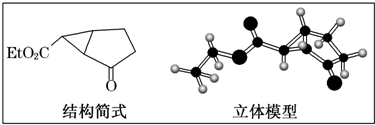
题目内容
下列离子方程式书写正确的是( )
| A、向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2═I2+2H2O |
| B、Cu片插入FeCl3溶液中:Cu+Fe3+═Fe2++Cu2+ |
| C、向Al2(SO4)3溶液中加入过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| D、向 NaHSO4溶液中滴加Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.发生氧化还原反应生成碘、水;
B.电子、电荷不守恒;
C.加入过量的氨水,生成硫酸铵、氢氧化铝;
D.滴加Ba(OH)2溶液至中性,生成硫酸钡、硫酸钠和水.
B.电子、电荷不守恒;
C.加入过量的氨水,生成硫酸铵、氢氧化铝;
D.滴加Ba(OH)2溶液至中性,生成硫酸钡、硫酸钠和水.
解答:
解:A.向海带灰浸出液中加入硫酸、双氧水的离子反应为2I-+2H++H2O2═I2+2H2O,故A正确;
B.Cu片插入FeCl3溶液中的离子反应为Cu+2Fe3+═2Fe2++Cu2+,故B错误;
C.Al2(SO4)3溶液中加入过量的氨水的离子反应为Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C错误;
D.向 NaHSO4溶液中滴加Ba(OH)2溶液至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选A.
B.Cu片插入FeCl3溶液中的离子反应为Cu+2Fe3+═2Fe2++Cu2+,故B错误;
C.Al2(SO4)3溶液中加入过量的氨水的离子反应为Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C错误;
D.向 NaHSO4溶液中滴加Ba(OH)2溶液至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选A.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
下列有关化学用语使用正确的是( )
A、硫原子的原子结构示意图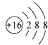 | ||
B、NH4Cl的电子式: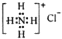 | ||
C、原子核内有10个中子的氧原子:
| ||
| D、基态铜原子的电子排布式为:1s22s22p63s23p63d94s2 |
下列各组中的离子或分子在指定溶液中一定能大量共存的是( )
| A、c(KNO3)=1.0mol/L的溶液中:Fe2+、Cl-、H+、Na+ | ||
| B、常温下,由水电离出的c(H+)=10-14mol/L溶液中:NH4+、CO32-、CH3COO-、SO42- | ||
| C、加入铝能产生大量氢气的溶液中:CH3CHO、MnO4-、K+、C6H5O- | ||
D、常温下,
|
据下表信息,判断以下叙述正确的是( )
| 部分短周期元素的原子半径及主要化合价 | ||||||
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
| A、GOH溶液和M(OH)3可以相互反应 |
| B、非金属性:T<Q |
| C、气态氢化物的稳定性:R>T |
| D、L2+与T2-核外电子数相等 |
X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构,下列说法中正确的是( )
| A、Y元素位于第二周期第ⅦA族或0族 |
| B、X、Y、Z三种元素中非金属性最强的是X元素 |
| C、X、Y、Z三种元素形成的简单离子的半径都比Mg2+半径小 |
| D、Z分别与X、Y形成的化合物都是离子化合物 |
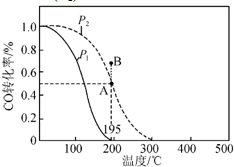 在20L的密闭容器中按物质的量之比1:2充入CO和H2,发生:CO(g)+2H2(g)?CH3OH(g);△H.测得CO的转化率随温度及不同压强下CO的变化如图所示,P2和195℃时n(H2)随时间的变化结果如表所示.下列说法正确的是( )
在20L的密闭容器中按物质的量之比1:2充入CO和H2,发生:CO(g)+2H2(g)?CH3OH(g);△H.测得CO的转化率随温度及不同压强下CO的变化如图所示,P2和195℃时n(H2)随时间的变化结果如表所示.下列说法正确的是( )P2及195℃n(H2)随时间变化
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
| A、P1<P2,△H<0 |
| B、0~3 min,平均速率v(CH3OH)=0.8 mol?L-1?min-1 |
| C、在P2及195℃时,该反应的平衡常数为25 L2?mol-2 |
| D、在B点时,v(正)>v(逆) |
不能用来说明Cl的非金属性比S强的是( )
| A、Cl的气态氢化物比S的稳定 |
| B、Cl原子最外层电子数比S原子最外层电子数多 |
| C、Cl2能从Na2S水溶液中置换S出来 |
| D、Cl的最高价氧化物的水化物酸性比S的强 |