题目内容
已知:H2(g)+F2(g)═2HF(g)△H=-270kJ?mol-1,下列说法正确的是( )
| A、2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 |
| B、1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
| C、在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
| D、1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
考点:有关反应热的计算
专题:
分析:A、由热化学方程式可知2mol氟化氢气体分解成1mol的氢气和1mol的氟气吸收270kJ热量;
B、液态氟化氢的能量比气态氟化氢的能量低,根据反应热与能量关系判断;
C、反应物总能量大于生成物的总能量为放热反应,反应物总能量小于生成物的总能量为吸热反应;
D、热化学方程式中化学计量数表示物质的量,不表示分子个数.
B、液态氟化氢的能量比气态氟化氢的能量低,根据反应热与能量关系判断;
C、反应物总能量大于生成物的总能量为放热反应,反应物总能量小于生成物的总能量为吸热反应;
D、热化学方程式中化学计量数表示物质的量,不表示分子个数.
解答:
解:A、由热化学方程式可知2mol氟化氢气体分解成1mol的氢气和1mol的氟气吸收270kJ热量,化学计量数表示物质的量,不是体积,故A错误;
B、液态氟化氢的能量比气态氟化氢的能量低,根据能量守恒,1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270kJ,故B错误;
C、反应为放热反应,在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量,故C正确;
D、热化学方程式中化学计量数表示物质的量,不表示分子个数,故D错误.
故选:C.
B、液态氟化氢的能量比气态氟化氢的能量低,根据能量守恒,1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270kJ,故B错误;
C、反应为放热反应,在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量,故C正确;
D、热化学方程式中化学计量数表示物质的量,不表示分子个数,故D错误.
故选:C.
点评:本题考查学生对热化学方程式的理解、反应热与能量关系,难度不大,注意反应物总能量大于生成物的总能量为放热反应,反应物总能量小于生成物的总能量为吸热反应.

练习册系列答案
相关题目
下列说法正确的是( )
| A、纤维素属于多糖,在人体内水解转化为葡萄糖,也可为人类提供能量 |
| B、糖尿病患者吃糖量必须限制,但淀粉类食物不必进行限制 |
| C、同质量的脂肪在体内氧化放出的能量比糖类和蛋白质高得多,是提供能量的主要物质 |
| D、葡萄糖在人体内不可以转化为脂肪,所以吃糖不会使人发胖 |
根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | KMnO4,HCl | Cl2、MnCl2… |
| A、第①组反应中,H2O2作还原剂 |
| B、第②组反应中,Cl2与FeBr2的物质的量之比为3:2 |
| C、第③组反应中,每生成1molCl2转移电子2mol |
| D、从三个反应可以得出:氧化性由强到弱顺序为MnO4->Fe3+>Cl2>Br2 |
下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是( )
①C与O2 ②Na与O2 ③Fe与Cl2 ④AlCl3溶液与NaOH溶液⑤CO2与NaOH溶液 ⑥Fe与硝酸.
①C与O2 ②Na与O2 ③Fe与Cl2 ④AlCl3溶液与NaOH溶液⑤CO2与NaOH溶液 ⑥Fe与硝酸.
| A、除③外 | B、除③⑤外 |
| C、除③④外 | D、除⑥外 |
20℃时,agKNO3溶于bg水中,恰好形成Vml饱和溶液.下列关系式错误的是( )
A、20℃时,KNO3的溶解度S=
| ||
B、该溶液的质量分数W (KNO3)=
| ||
C、该溶液的物质的量浓度C (KNO3)=
| ||
D、该溶液的密度ρ=
|
将一定量的Na2SO4溶于90ml水中,使得每100个水分子中溶有一个Na+,这一定量的Na2SO4是 (( )
| A、142g |
| B、71g |
| C、0.05mol |
| D、0.025mol |
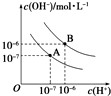 已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示:
已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示: