题目内容
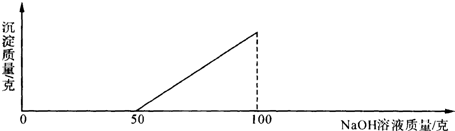
 请根据如图所示实验过程和数据计算:
请根据如图所示实验过程和数据计算:(1)反应中生成氢气的质量.
(2)反应后溶液中硫酸的质量为多少克.
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Zn+H2SO4=ZnSO4+H2↑,根据方程式计算生成氢气的质量、参加反应的硫酸的质量,根据质量守恒计算原硫酸溶液的质量,再根据质量分数计算原硫酸溶液中硫酸的质量,进而计算反应后溶液中硫酸的质量.
解答:
解:设生成氢气的质量为x,参加反应的H2SO4的质量为y,则:
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g y x
所以x=
=0.4g y=
=19.6g
设原硫酸溶液的质量为z,则z+13g-0.4g=162.6g,解得z=150g,
故剩余H2SO4的质量=150g×20%-19.6g=10.4g,
答:(1)生成氢气的质量为0.4g.
(2)剩余硫酸的质量为10.4g.
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g y x
所以x=
| 13g×2 |
| 65 |
| 13g×98 |
| 65 |
设原硫酸溶液的质量为z,则z+13g-0.4g=162.6g,解得z=150g,
故剩余H2SO4的质量=150g×20%-19.6g=10.4g,
答:(1)生成氢气的质量为0.4g.
(2)剩余硫酸的质量为10.4g.
点评:本题考查化学方程式的有关计算,难度不大,计算原硫酸溶液的质量是关键.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
下列事故处理正确的是( )
| A、苯酚沾在手上立即用酒精洗涤 |
| B、误食铜盐立即喝牛奶或蛋清 |
| C、鱼、肉等食品用福尔马林浸泡防腐保鲜 |
| D、皮肤沾上了浓HNO3而变黄色,立即用饱和NaOH溶液冲洗 |
以下说法正确的是( )
| A、16O转化为18O不是化学变化 |
| B、汽车尾气中的CO、NO等都是汽油和柴油的不完全燃烧产物 |
| C、t℃时,1L pH=6的纯水中OH-的数目为10-8NA |
| D、同一物质不同聚集状态下分子间的平均距离都是:d(气态)>d(液态)>d(固态) |
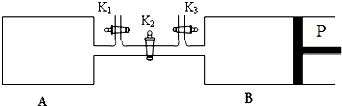
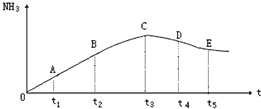 在容积不变的密闭容器中,分别充入1.0mol N2和3.0molH2,任其发生反应:
在容积不变的密闭容器中,分别充入1.0mol N2和3.0molH2,任其发生反应: