题目内容
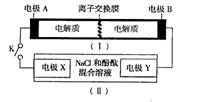
 如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3═K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红.则闭合K时,下列说法正确的是( )
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3═K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红.则闭合K时,下列说法正确的是( )分析:当闭合开关K时,X附近溶液先变红,说明X极生成OH-,应为电解池的阴极,发生反应为:2H2O+2e-=H2↑+2OH-,Y为电解池的阳极,发生:2Cl--2e-═Cl2↑,则A为原电池的负极,电极反应式为2K2S2-2e-═K2S4+2K+,B为原电池的正极,电极反应式为I3-+2e-═3I-,以此解答该题.
解答:解:当闭合开关K时,X附近溶液先变红,说明X极生成OH-,应为电解池的阴极,发生反应为:2H2O+2e-=H2↑+2OH-,Y为电解池的阳极,发生:2Cl--2e-═Cl2↑,则A为原电池的负极,电极反应式为2K2S2-2e-═K2S4+2K+,B为原电池的正极,电极反应式为I3-+2e-═3I-,
A.钾离子向正极移动,则钾离子向B电极移动,故A错误;
B.A为负极,失电子发生氧化反应,电极反应式为2K2S2-2e-═K2S4+2K+,故B错误;
C.X电极上得电子发生还原反应,电极反应式为2H2O+2e-=H2+2OH-,故C错误;
D.当有0.1 mol K+通过离子交换膜,根据2K2S2-2e-═K2S4+2K+知,转移电子的物质的量是0.1mol,根据转移电子守恒知,X电极上产生气体体积=
×22.4L/mol=1.12L,故D正确.
故选D.
A.钾离子向正极移动,则钾离子向B电极移动,故A错误;
B.A为负极,失电子发生氧化反应,电极反应式为2K2S2-2e-═K2S4+2K+,故B错误;
C.X电极上得电子发生还原反应,电极反应式为2H2O+2e-=H2+2OH-,故C错误;
D.当有0.1 mol K+通过离子交换膜,根据2K2S2-2e-═K2S4+2K+知,转移电子的物质的量是0.1mol,根据转移电子守恒知,X电极上产生气体体积=
| 0.1mol |
| 2 |
故选D.
点评:本题考查了原电池和电解池原理,以X电极现象确定电解池阴阳极,从而确定原电池正负极,再结合各个电极上得失电子书写电极反应式,难点是电极反应式的书写,难度中等.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
如图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3  K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )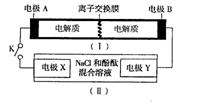
| A.K+从右到左通过离子交换膜 |
| B.电极A上发生的反应为:3I--2e-=I3- |
| C.电极X上发生的反应为:2Cl--2e-=C12↑ |
| D.当有0.1 mol K+通过离子交换膜,X电极上产生1.12 L气体(标准状况) |
 K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是 ( )