题目内容
15.A、B、C、D为短周期元素.A的一种原子无中子,B原子的最外层电子数是内层电子数的两倍,A与C能形成原子个数比为1:1和2:1的两种化合物,D的气态氢化物与其最高价氧化物的水化物反应生成盐.(1)用电子式表示A与C形成的原子个数比为2:1的化合物的过程:
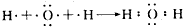 .
.(2)D的氢化物的沸点比同主族其他元素的氢化物的沸点都要高,其原因是:NH3分子间能形成氢键.
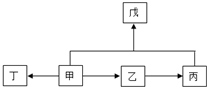 (3)A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,其存在如图转化关系:
(3)A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,其存在如图转化关系:①若丁的产量可以用来衡量一个国家石油化工的发展水平,写出由甲制得丁的反应化学方程式
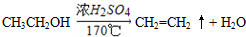 ;
;②甲与丙的制取戊的反应条件为浓硫酸、加热,实验室用饱和碳酸钠溶液吸收该反应的产品,饱和碳酸钠溶液的具体作用是:溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度.
(4)蛋白质是重要的营养物质,其最终水解产物为氨基酸(或α-氨基酸),A、B、C、D四种元素可以形成一种最简单的该类物质,其结构简式为NH2CH2COOH或
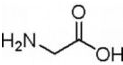 .
.
分析 A的一种原子无中子,为H元素,B原子的最外层电子数是内层电子数的两倍,为C元素,A与C能形成原子个数比为1:1和2:1的两种化合物,C为O元素,形成的化合物分别为H2O、H2O2,D的气态氢化物与其最高价氧化物的水化物反应生成盐,为N元素,
A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,若丁的产量可以用来衡量一个国家石油化工的发展水平,应为乙烯,则甲为乙醇,乙为乙醛,丙为乙酸,戊为乙酸乙酯,以此解答该题.
解答 解:A的一种原子无中子,为H元素,B原子的最外层电子数是内层电子数的两倍,为C元素,A与C能形成原子个数比为1:1和2:1的两种化合物,C为O元素,形成的化合物分别为H2O、H2O2,D的气态氢化物与其最高价氧化物的水化物反应生成盐,为N元素,
(1)A与C形成的原子个数比为2:1的化合物为水,电子式表示的形成过程为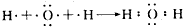 ,故答案为:
,故答案为: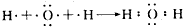 ;
;
(2)N的非金属性较强,对应的氨气分子间可形成氢键,作用力较强,则沸点较高,故答案为:NH3分子间能形成氢键;
(3)A、B、C三种元素能形成多种化合物.某化合物甲一分子中含有一个氧原子,相对分子质量为46,若丁的产量可以用来衡量一个国家石油化工的发展水平,应为乙烯,则甲为乙醇,乙为乙醛,丙为乙酸,戊为乙酸乙酯,
①乙醇在浓硫酸作用下发生消去反应生成乙烯,方程式为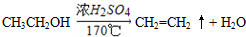 ,
,
故答案为: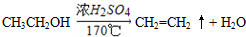 ;
;
②乙酸乙酯不溶于饱和碳酸钠溶液,且乙醇易溶于水,乙酸可与碳酸钠反应,故答案为:溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度;
(4)蛋白质的最终水解产物为氨基酸,最简单的氨基酸为NH2CH2COOH或 ,
,
故答案为:氨基酸(或α-氨基酸);NH2CH2COOH或 .
.
点评 本题综合考查元素化合物、原子周期表以及有机物的推断,为高频考点,侧重于学生的分析能力的考查,注意把握原子结构以及有机物的结构和性质,难度不大.

| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | ↓ | ↓↑ | ↓ | ↓ | ↑ |
| A. | AlCl3、HCl、AgNO3、Na2CO3 | B. | AgNO3、HCl、Na2CO3、AlCl3 | ||
| C. | Na2CO3、AlCl3、HCl、AgNO3 | D. | AgNO3、HCl、AlCl3、Na2CO3 |
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 酸性高锰酸钾溶液应装在酸式滴定管中,原因是酸性高锰酸钾能氧化橡胶 | |
| C. | 植物油和裂化汽油都能使溴水褪色,原理是不同的 | |
| D. | 明矾能够用于净水,是因为明矾的溶液是酸性的 |
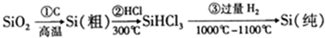 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 步骤①的化学方程式为:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1mol Si,转移2mol电子 | |
| C. | 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
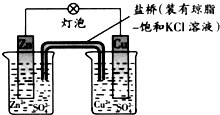
| A. | 正极反应为:Zn-2e-═Zn2+ | B. | 在外电路中,电子从铜片流向锌片 | ||
| C. | 负极发生还原反应 | D. | 盐桥中的K+移向CuSO4溶液 |