题目内容
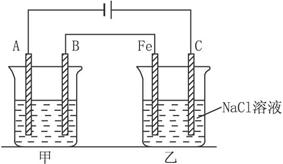
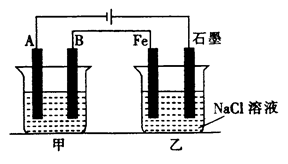
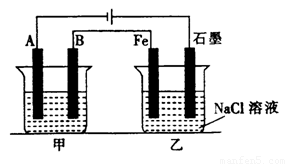
如下图所示:甲、乙为相互串联的两电解池。
试回答:
(1)乙池中Fe极电极反应式为______________,若在乙池中滴入少量酚酞试液,开始电解一段时间,铁极附近呈_________色。
(2)甲池若为用电解原理精炼铜(假设粗铜的组成
是均匀的,且比其活泼和不活泼的成分均存在)
的装置,则A电极名称为__________极,电极反应式为______________,电解质溶液可以是______________;通电一段时间后,A极增重12.8 8,则甲池溶液原溶质的浓度(填“增大”减小”不变”或“无法确定”),乙池C(石墨)极放出气体在标况下的体积为____________,此时乙池剩余溶液的体积为400mL,则溶液的pH=__________。
(1)2H++2e-====H2↑ 红
(2)阴 Cu2++2e-====Cu
CuSO4溶液或CuCl2溶液 不变
4.48L 14
解析:本题考查电解原理及其应用(粗铜的精炼和电解饱和食盐水)。
乙池中Fe为阴极,溶液中H+放电形成H2放出,溶液中[OH-]提高,故显碱性,滴入酚酞变红。
甲池若为电解原理精炼Cu装置,则A极为精Cu,B极为粗Cu,阴极反应:Cu2+2e-=Cu,阳极反应:Cu-2e-=Cu由于阴极析出Cu的质量等于阳极溶解Cu的质量,故电解液浓度保持不变。
甲池中:
A极:Cu2++2e-====Cu
2 mol 64 g
x 12.8 g x=0.4 mol
乙池中:
2NaCl+2H2O![]() 2NaOH+H2↑+Cl↑—2e-
2NaOH+H2↑+Cl↑—2e-
2 mol 22.4L 2 mol
Z Y 0.4 mol
Y=4.48 L Z=0.4 mol


 导学全程练创优训练系列答案
导学全程练创优训练系列答案