题目内容
下列关于电解质溶液的叙述正确的是( )
| A、常温下,由0.1mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH?B++OH- |
| B、常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
考点:电解质在水溶液中的电离
专题:电离平衡与溶液的pH专题
分析:A、弱电解质在水中液中不能完全电离;
B、pH=7的NH4Cl与氨水的混合溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(NH4+)+c(H+),据此判断;
C、pH与体积均相同的盐酸和醋酸溶液,醋酸的物质的量大,据此回答;
D、将pH=4的盐酸稀释后,酸性减弱,但是水的离子积是定值.
B、pH=7的NH4Cl与氨水的混合溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(NH4+)+c(H+),据此判断;
C、pH与体积均相同的盐酸和醋酸溶液,醋酸的物质的量大,据此回答;
D、将pH=4的盐酸稀释后,酸性减弱,但是水的离子积是定值.
解答:
解:A、常温下,由0.1mol/L一元碱BOH溶液的pH=10,则证明BOH溶液在水中液中不能完全电离,是一种弱碱,存在电离平衡:BOH?B++OH-,故A正确;
B、NH4Cl与氨水的混合溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(NH4+)+c(H+),pH=7,即c(H+)=c(OH-),c(Cl-)=c(NH4+),即c(Cl-)>c(NH4+)>c(H+)=c(OH-),故B错误;
C、pH与体积均相同的盐酸和醋酸溶液,醋酸的物质的量大,所以醋酸消耗的氢氧化钠的量多,故C错误;
D、将pH=4的盐酸稀释后,酸性减弱,c(H+)减小,但是水的离子积Kw=c(H+)?c(OH-),是定值,所以c(OH-)增大,故D错误.
故选A.
B、NH4Cl与氨水的混合溶液中存在电荷守恒:c(Cl-)+c(OH-)=c(NH4+)+c(H+),pH=7,即c(H+)=c(OH-),c(Cl-)=c(NH4+),即c(Cl-)>c(NH4+)>c(H+)=c(OH-),故B错误;
C、pH与体积均相同的盐酸和醋酸溶液,醋酸的物质的量大,所以醋酸消耗的氢氧化钠的量多,故C错误;
D、将pH=4的盐酸稀释后,酸性减弱,c(H+)减小,但是水的离子积Kw=c(H+)?c(OH-),是定值,所以c(OH-)增大,故D错误.
故选A.
点评:本题考查学生弱电解质的电离以及离子浓度之间的关系知识,属于综合知识的考查,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
利用下列实验装置进行的相应实验,不能达到实验目的是( )


| A、图1所示装置可制取乙炔 |
| B、图2所示装置可分离乙酸乙酯和醋酸钠的水溶液 |
| C、图3所示装置可制取乙烯并验证其易被氧化 |
| D、图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
下列叙述中正确的是( )
| A、NH3、CO、CO2都是极性分子 |
| B、CH4、CO2都是含有极性键的非极性分子 |
| C、HF、HCl、HBr的沸点依次增强 |
| D、CS2、H2O、C2H2都是直线型分子 |
燃气灶中心的金属容易生锈,这说明化学腐蚀速率与( )有关.
| A、催化剂 | B、温度 |
| C、反应物本性 | D、气体浓度 |
铝土矿的主要成分是Al2O3、Fe2O3、SiO2等,从铝土矿冶炼Al2O3的流程如下:
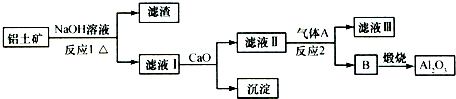
下列说法正确的是( )

下列说法正确的是( )
| A、气体A一定为HCl |
| B、滤液Ⅰ中溶质仅含NaAlO2 |
| C、沉淀的主要成分为硅酸钙 |
| D、反应1、反应2均不是氧化还原反应 |