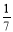题目内容
(14分)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____,该反应的还原产物是_____。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是_____,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是_____mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_____ mol,参加反应的硝酸的物质的量是_____mol,产生的混合气体中NO和NO2体积比为_______。
(14分)(1) 酸性和氧化性(2分);NO和NO2(2分) ;(2) 0.8NA(2分) ;1.2mol(2分) ;(3)0.4 (2分) ;1mol(2分) ;1:3(2分);
【解析】
试题分析:(1)硝酸在该反应中氮元素化合价降低表现出氧化性,生成硝酸铜与水表现出酸性,该反应的还原产物是NO和NO2气体。
(2)由得失电子守恒,硝酸得到的电子数等于铜失去电子数是0.4mol×2=0.8mol,即0.8NA,如果得到的NO和NO2物质的量相同,则氮元素平均降2价,得2个电子,参加反应的硝酸的物质的量是0.8mol÷2=0.4mol。
(3)由氮原子守恒,被还原的硝酸的物质的量是生成NO和NO2的物质的量即8.96L÷22.4L/mol=0.4 mol,生成硝酸铜0.3mol,消耗硝酸0.6mol,参加反应的硝酸的物质的量是0.4mol+0.6mol=1mol,设产生的混合气体中NO和NO2的物质的量分别为x、y 则x+y=0.4mol ,由得失电子守恒得,3x+y=0.6mol,解得x=0.1mol,y=0.3mol,产生的混合气体中NO和NO2体积比为1:3。
考点:通过铜与硝酸的反应考查氧化还原反应


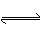 2SO3(g),在不同条件下测得化学反应速率最快的为
2SO3(g),在不同条件下测得化学反应速率最快的为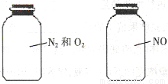
 2HI(g)的平衡常数是49,则
2HI(g)的平衡常数是49,则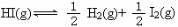 ,在该温度下的平衡常数是
,在该温度下的平衡常数是 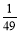 B.7 C.2401 D.
B.7 C.2401 D.