题目内容
物质的转化关系如图所示,其中甲可由两种单质直接化合得到,乙为金属单质,F的溶液中只含一种溶质,G为酸,乙在G的浓溶液中发生钝化.有的反应可能在水溶液中进行,有的反应中生成物未全部给出,反应条件也未注明.
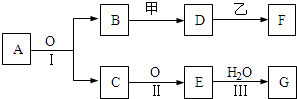
(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性.则
①1.7g A与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式: .
②B与甲反应的离子方程式是 .
(2)若B为红棕色固体,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成.则
①工业上反应Ⅰ在 中进行,反应Ⅲ在 (均填设备名称)中进行.
②D和乙反应的离子方程式是 .

(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性.则
①1.7g A与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式:
②B与甲反应的离子方程式是
(2)若B为红棕色固体,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成.则
①工业上反应Ⅰ在
②D和乙反应的离子方程式是
考点:无机物的推断
专题:推断题
分析:(1)甲为一种淡黄色固体,且为化合物,应为Na2O2,若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成,G为酸,应为HNO3(或HCl)和NH3的反应,由于G是由A经过两步氧化后得到的,所以G为HNO3,生成NH4NO3,且A能与O2反应,应为NH3,则C为NO,E为NO2,乙在G的浓溶液中发生钝化,则乙为铝或铁,能与NaOH反应的金属则为Al,所以乙为Al,B为H2O,与Na2O2反应生成NaOH,F为NaAlO2,
(2)B、C是A 的氧化产物,且B为红棕色固体,则B为Fe2O3,C能使品红试液褪色,则C为SO2,结合转化关系可推知,E为SO3,G为H2SO4,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成,说明D中含有Cl-,可推知甲为HCl,D为FeCl3,乙在浓硫酸中发生钝化,应为Fe,与氯化铁溶液反应生成F,F的溶液中只含有一种溶质,则F为FeCl2,据此答题.
(2)B、C是A 的氧化产物,且B为红棕色固体,则B为Fe2O3,C能使品红试液褪色,则C为SO2,结合转化关系可推知,E为SO3,G为H2SO4,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成,说明D中含有Cl-,可推知甲为HCl,D为FeCl3,乙在浓硫酸中发生钝化,应为Fe,与氯化铁溶液反应生成F,F的溶液中只含有一种溶质,则F为FeCl2,据此答题.
解答:
解:(1)甲为一种淡黄色固体,且为化合物,应为Na2O2,若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成,G为酸,应为HNO3(或HCl)和NH3的反应,由于G是由A经过两步氧化后得到的,所以G为HNO3,生成NH4NO3,且A能与O2反应,应为NH3,则C为NO,E为NO2,乙在G的浓溶液中发生钝化,则乙为铝或铁,能与NaOH反应的金属则为Al,所以乙为Al,B为H2O,与Na2O2反应生成NaOH,F为NaAlO2,
①1.7g 氨气即为0.1mol,与O2反应生成气态的B和C时放出22.67kJ热量,则4mol氨气反应可以放出106.8KJ的热,该反应的热化学方程式为4NH3(g)+5O2(g)
4NO(g)+6H2O(g)△H=-106.8kJ/mol,
故答案为:4NH3(g)+5O2(g)
4NO(g)+6H2O(g);△H=-106.8kJ/mol;
②水与过氧化钠反应的离子方程式是为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(2)B、C是A 的氧化产物,且B为红棕色固体,则B为Fe2O3,C能使品红试液褪色,则C为SO2,结合转化关系可推知,E为SO3,G为H2SO4,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成,说明D中含有Cl-,可推知甲为HCl,D为FeCl3,乙在浓硫酸中发生钝化,应为Fe,与氯化铁溶液反应生成F,F的溶液中只含有一种溶质,则F为FeCl2,
①工业上反应Ⅰ是冶炼铁的反应的第一步,在沸腾炉中进行,反应Ⅲ是三氧化硫生成硫酸的过程,是在吸收塔中进行,故答案为:沸腾炉;吸收塔;
②FeCl3和铁反应的离子方程式是2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+.
①1.7g 氨气即为0.1mol,与O2反应生成气态的B和C时放出22.67kJ热量,则4mol氨气反应可以放出106.8KJ的热,该反应的热化学方程式为4NH3(g)+5O2(g)
| ||
| △ |
故答案为:4NH3(g)+5O2(g)
| ||
| △ |
②水与过氧化钠反应的离子方程式是为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(2)B、C是A 的氧化产物,且B为红棕色固体,则B为Fe2O3,C能使品红试液褪色,则C为SO2,结合转化关系可推知,E为SO3,G为H2SO4,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成,说明D中含有Cl-,可推知甲为HCl,D为FeCl3,乙在浓硫酸中发生钝化,应为Fe,与氯化铁溶液反应生成F,F的溶液中只含有一种溶质,则F为FeCl2,
①工业上反应Ⅰ是冶炼铁的反应的第一步,在沸腾炉中进行,反应Ⅲ是三氧化硫生成硫酸的过程,是在吸收塔中进行,故答案为:沸腾炉;吸收塔;
②FeCl3和铁反应的离子方程式是2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+.
点评:本题考查无机物的推断,颜色、特殊性质、反应现象为推断的突破口,侧重于学生分析能力与元素化合物知识的考查,难度中等.

练习册系列答案
相关题目
氯化硼的熔点为107℃.在氯化硼分子中,氯硼键之间的夹角为120°,它可水解,水解产物之一能在空气中产生白雾.下列关于氯化硼的说法正确的是( )
| A、氯化硼是原子晶体 |
| B、氯化硼分子是极性分子 |
| C、熔化时,氯化硼能导电 |
| D、水解方程式:BCl3+3H2O=H3BO3+3HCl |
将CO2和C加入密闭容器中,在一定条件下发生反应:CO2(g)+C(s)?2CO(g),忽略固体体积,平衡时CO的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是( )
| 温度/℃ CO的体积分数/% 压强/MPa | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 80.0 |
| A、b<f |
| B、900℃,2.0MPa的转化率为60% |
| C、K(1000℃)=3.2 |
| D、K(1000℃)>K(800℃) |