题目内容
14.下列电子式书写正确的是( )| A. | 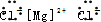 | B. |  | C. | 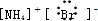 | D. | 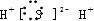 |
分析 A.氯化镁属于离子化合物的,镁离子直接用离子符号表示,氯离子需要标出最外层电子及所带电荷;
B.Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子;
C.溴化铵为离子化合物,电子式中需要标出阴阳离子所带电荷和阴阳离子的电子式;
D.硫化氢为共价化合物,不带电荷.
解答 解:A.氯化镁属于离子化合物的,镁离子直接用离子符号表示,氯离子需要标出最外层电子及所带电荷,两个氯离子写在镁离子的两边,氯化镁制取的电子式为: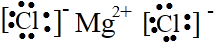 ,故A错误;
,故A错误;
B.Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为 ,故B正确;
,故B正确;
C.溴化铵为离子化合物,溴离子需要标出最外层电子,溴化钠正确的电子式为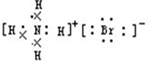 ,故C错误;
,故C错误;
D.硫化氢为共价化合物,不带电荷,正确的电子式为: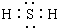 ,故D错误.
,故D错误.
故选B.
点评 本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
5.近年,科学家发现了116号元素Lv.下列关于293Lv和294Lv的说法错误的是( )
| A. | 两者电子数相差1 | B. | 两者质量数相差1 | C. | 两者中子数相差1 | D. | 两者互为同位素 |
2.下列物质分类正确的是( )
①混合物:铝热剂、碱石灰、水玻璃、漂白粉; ②化合物:氯化钙、烧碱、胆矾、冰水混合物
③酸性氧化物:Mn2O7、N2O3、SiO2、NO2 ④碱性氧化物:Na2O2、CuO、Al2O3、MgO
⑤同素异形体:C60、C70、金刚石、石墨 ⑥强电解质:AlCl3、BaSO4、MgO、Ba(OH)2.
①混合物:铝热剂、碱石灰、水玻璃、漂白粉; ②化合物:氯化钙、烧碱、胆矾、冰水混合物
③酸性氧化物:Mn2O7、N2O3、SiO2、NO2 ④碱性氧化物:Na2O2、CuO、Al2O3、MgO
⑤同素异形体:C60、C70、金刚石、石墨 ⑥强电解质:AlCl3、BaSO4、MgO、Ba(OH)2.
| A. | ①②⑤⑥ | B. | ②③④⑥ | C. | ①②④⑤ | D. | ①②④⑥ |
9.在一定条件下,在体积为VL的密闭容器中发生反应:mA+nB?pC.t秒末,A减少了1mol,B减少了1.25mol,C增加了0.5mol.则m:n:p应为( )
| A. | 4:5:2 | B. | 2:5:4 | C. | 1:3:2 | D. | 3:2:1 |
19.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1 molCu和足量热浓硫酸反应可生成NA个SO3分子 | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
6.下列物质组合中,既能和酸反应又能和碱反应的化合物是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3.
| A. | ①②③⑤ | B. | ①②③④⑤ | C. | ①③⑤ | D. | ②③④ |
3.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成大量的SO3 | |
| B. | SO2能使品红溶液、酸性KMnO4溶液褪色,褪色原理相同 | |
| C. | 可以用品红溶液鉴别SO2和CO2 | |
| D. | 少量SO2通过CaCl2的溶液能生成白色沉淀 |
4.在同温、同压下,相同物质的量的氢气和氦气,具有相同的( )
| A. | 原子数 | B. | 质子数 | C. | 体积 | D. | 质量 |

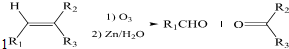

 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).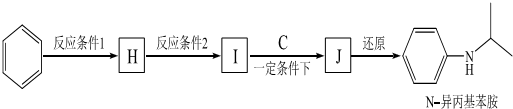
 .
.