题目内容
1.在过滤操作过程中,不需用到的玻璃仪器为( )| A. | 漏斗 | B. | 烧杯 | C. | 玻璃棒 | D. | 酒精灯 |
分析 过滤需要烧杯、漏斗、玻璃棒,以此来解答.
解答 解:过滤分离溶液与不溶性固体,在铁架台上放漏斗,漏斗下方为烧杯,然后利用玻璃棒引流,进行过滤操作,不需要酒精灯,
故选D.
点评 本题考查过滤实验操作,为高频考点,把握过滤装置及需要的仪器为解答的关键,侧重分析与应用能力的考查,注意常见仪器的使用,题目难度不大.

练习册系列答案
相关题目
11.在一定条件下,四个体积相同的密闭容器中,发生反应2SO2+O2$?_{△}^{催化剂}$2SO3,反应速率最快的是( )
| 容器 | 温度/℃ | SO2/mol | O2/mol | 催化剂 |
| A | 400 | 4 | 2 | 无 |
| B | 400 | 2 | 1 | 无 |
| C | 500 | 2 | 1 | 无 |
| D | 500 | 4 | 2 | 有 |
| A. | A | B. | B | C. | C | D. | D |
12.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下,11.2L二氧化硫所含的氧原子数等于NA | |
| B. | 0.5molH2O所含的电子数为9NA | |
| C. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| D. | 300mL2mol•L-1蔗糖溶液中所含分子数为0.6NA |
9.下列说法正确的是( )
| A. | 常温下,某溶液中由水电离出来的 c(H+)=1×10-amol•L-1,若 a<7,则该溶液可能为 NaHSO4溶液 | |
| B. | 中和同体积、同 pH 的硫酸、盐酸和醋酸所需相同浓度的 NaOH 溶液的体积关系:V(硫酸)>V(盐酸)>V(醋酸) | |
| C. | 向 AgCl 悬浊液中加入 NaCl 固体,AgCl 沉淀的溶度积(Ksp)变小 | |
| D. | pH 相等的①CH3COONa ②NaHCO3溶液中,c(Na+)大小关系:②<① |
16.下列物质的用途,利用了物质的氧化性的是( )
| A. | 用食盐腌渍食物 | B. | 用钠制过氧化钠 | ||
| C. | 用过氧化钠漂白织物 | D. | 用碳酸氢钠治疗胃酸过多 |
6.下列离子方程式中正确的是( )
| A. | H2SO4与 Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | Ca(HCO3)2与过量 NaOH 溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | Na2CO3溶液中通入少量 CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | CH3COOH 溶液与 NaOH 溶液反应:H++OH-═H2O |
13.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol及b mol碘化氢(a>b),待反应2HI(g)?I2(g)+H2(g) 达平衡后,下列说法正确的是( )
| A. | 平衡时两容器中I2的物质的量相等 | |
| B. | 平衡时两容器中I2的浓度相等 | |
| C. | 平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器 | |
| D. | 平衡时HI的分解率:αA=αB |
10.25℃时,下列有关0.1mol•L-1醋酸溶液的说法中,正确的是( )
| A. | pH=1 | |
| B. | c(H+)=c(CH3COO-) | |
| C. | 加入少量CH3COONa固体后,醋酸的电离程度减小 | |
| D. | 与0.1 mol•L-1NaOH溶液等体积混合后所得溶液显中性 |
11.某待测溶液(阳离子为Na+)中可能含有SO42-、SO32-、NO3-、Cl-、Br-、CO32-、HCO3-中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,已知稀HNO3有强氧化性,下列说法不正确的是( )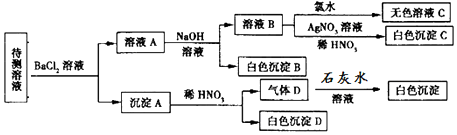

| A. | SO42-、SO32-至少含有一种 | |
| B. | 沉淀B的化学式为BaCO3 | |
| C. | 肯定存在的阴离子有CO32-、HCO3-、Cl- | |
| D. | 肯定没有的离子是Br- |