题目内容
下列装置不能完成的实验是( )
| A | B | C | D | |
| 装置 | 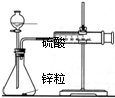 | 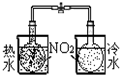 | 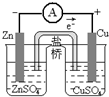 |  |
| 实验 | 结合秒表测量锌与硫酸的反应速率 | 验证温度对化学平衡的影响 | 验证化学能转化为电能 | 铁的析氢腐蚀实验 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.气体的体积可由注射器量出;
B.已知2NO2?N2O4△H<0,根据颜色的变化判断;
C.图中可形成原电池;
D.食盐水呈中性.
B.已知2NO2?N2O4△H<0,根据颜色的变化判断;
C.图中可形成原电池;
D.食盐水呈中性.
解答:
解:A.气体的体积可由注射器量出,结合时间可求出反应速率,故A正确;
B.已知2NO2?N2O4△H<0,根据颜色的变化可知平衡移动的方向,以此可确定温度对平衡移动的影响,故B正确;
C.图中可形成原电池,能产生电流,指针发生偏转,故C正确;
D.食盐水呈中性,发生吸氧腐蚀,故D错误.
故选D.
B.已知2NO2?N2O4△H<0,根据颜色的变化可知平衡移动的方向,以此可确定温度对平衡移动的影响,故B正确;
C.图中可形成原电池,能产生电流,指针发生偏转,故C正确;
D.食盐水呈中性,发生吸氧腐蚀,故D错误.
故选D.
点评:本题考查较为综合,涉及化学反应速率的测定、化学平衡移动、原电池以及金属的腐蚀等知识,侧重于学生的分析能力和额实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
下列关于元素在周期表中位置的叙述正确的是( )
| A、原子的最外层有2个电子的元素一定是ⅡA族元素 | ||
| B、元素所在的主族序数与最外层电子数之比为1的元素都是金属元素 | ||
C、俄罗斯专家首次合成了
| ||
| D、原子最外层电子数大于3(小于8)的元素一定是非金属元素 |
已知第二周期和第三周期元素形成的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、离子半径:C3->D->B+>A2+ |
| B、原子序数:d>c>b>a |
| C、原子半径:A>B>D>C |
| D、原子的最外层电子数目:A>B>D>C |
常温下,下列各组微粒在指定的分散系中一定能大量共存的是( )
| A、由水电离出的c(OH-)=1×10-13mol/L的溶液:Na+、Ba2+、Cl-、Br- |
| B、使甲基橙呈黄色的溶液:NO3-、I-、Na+、Cl- |
| C、含CO32-的溶液:Al3+、K+、Cl-、SO42- |
| D、鸡蛋清水溶胶:甲醛分子、蔗糖分子、甘油分子、Na+、Cl- |
区分晶体和非晶体的最科学的方法是( )
| A、测固体的熔点 |
| B、看固体是否易被压缩 |
| C、对固体进行X射线衍射实验 |
| D、比较固体的导热性 |
| E、比较固体的导热性 |
一定温度下,密闭体积的容器中进行反应4A(g)+6B(g)?4C(g)+5D(g),则下列有关化学反应速率的关系正确的是( )
| A、4v(A)=6v(B) | ||
| B、6v(B)=5v (D) | ||
C、v(C)=
| ||
D、v(A)=
|
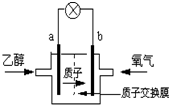 圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )
圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )| A、a极为电池的正极 |
| B、电池正极的电极反应为:4H++O2+4e-═2H2O |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池工作时,1mol乙醇被氧化时就有6 mol电子转移 |
从海水中提取镁的工艺流程主体是( )
A、海水
| ||||||
B、海水
| ||||||
C、海水
| ||||||
D、海水
|