题目内容
【题目】下列说法中正确的是
A.远洋货轮船体上加装的锌板需定期更换
B.铁表面镀锌时,铁与直流电源的正极相连
C.镀层破损后,镀锌铁板比镀锡铁板更易腐蚀
D.电解精炼铜时,电解质溶液的组成保持不变
【答案】A
【解析】
A.金属在海水中容易发生电化学腐蚀,远洋货轮船体上加装锌板,为牺牲阳极的阴极保护法,则锌需要定期更换,A正确;
B. 铁表面镀锌时,铁与直流电源的负极相连,B错误;
C. 镀层破损后,镀锌铁,锌作电池的负极失电子变为离子,铁作正极被保护;镀锡铁,铁作负极被腐蚀,镀锌铁板比镀锡铁板更耐腐蚀,C错误;
D. 电解精炼铜时,粗铜中含有的锌、铁等变为离子成为电解质溶液的一部分,D错误;
答案为A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= , 已知:K(300℃)>K(350℃),该反应是反应(填“放热”或“吸热”). 
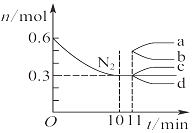
(2)图中表示NO2的变化的曲线是 , 用O2的浓度变化表示从0~2s内该反应的平均速率v= .
(3)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂.