题目内容
16.氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答下列问题:I.把氯气通入紫色石蕊溶液中,可以观察到的现象是:溶液变为红色,然后褪色;
请你解释其中的原因氯气溶液水生成盐酸和次氯酸,使溶液呈酸性,紫色石蕊溶液遇到酸显红色,生成的次氯酸具有漂白性,能够使变红的石蕊褪色.
Ⅱ.某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液.
(1)其反应原理为:Cl2+2OH-═Cl-+ClO-+H2O(用离子方程式表示).
(2)实验室配制好4.0mol•L-1的NaOH溶液,这种溶液0.05L才能与2.24L氯气(STP)恰好完全反应.
(3)配制100mL4.0mol•L-1NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量.
b.称量氢氧化钠固体.
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶.
d.用适量蒸馏水溶解称量好的氢氧化钠固体,冷却.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切.
①配制过程中不需要用到的仪器是D.
A.烧杯 B.玻璃棒 C.100mL容量瓶 D.锥形瓶
②上述步骤的正确操作顺序是abdcfe.
③所需称量的氢氧化钠固体的质量是16.0g.
④配制过程中出现以下情况,对所配制溶液浓度无影响的是C.
A.没有洗涤烧杯和玻璃棒.
B.如果加水超过了刻度线,取出水使液面恰好到刻度线.
C.容量瓶没有干燥.
分析 I.依据氯气与水反应生成产物的性质判断解答:
Ⅱ.(1)氯气和氢氧化钠反应生成NaCl、NaClO、水;
(2)依据方程式Cl2+2NaOH=NaCl+NaClO+H2O及物质的量计算解答;
(3)①依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
②依据配制一定物质的量浓度溶液一般步骤排序;
③依据m=CVM计算需要溶质的质量;
④分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:I.氯气溶液水生成盐酸和次氯酸,使溶液呈酸性,紫色石蕊溶液遇到酸显红色,生成的次氯酸具有漂白性,能够使变红的石蕊褪色,所以看到现象为:溶液变为红色,然后褪色;
故答案为:溶液变为红色,然后褪色;氯气溶液水生成盐酸和次氯酸,使溶液呈酸性,紫色石蕊溶液遇到酸显红色,生成的次氯酸具有漂白性,能够使变红的石蕊褪色;
Ⅱ.(1)氯气和氢氧化钠反应生成NaCl、NaClO、水,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O;
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(2)n(Cl2)=$\frac{2.24L}{22.4L/mol}$=0.1mol
由Cl2+2NaOH=NaCl+NaClO+H2O
知n(NaOH)=2n(Cl2)=2×0.1mol=0.2mol
V(NaOH溶液)=$\frac{0.2L}{4.0mol/L}$=0.05L,
故答案为:0.05;
(3)①配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等用到的仪器:烧杯、玻璃棒、100mL容量瓶、胶头滴管,用不到的仪器:锥形瓶;
故答案为:D;
②配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,正确的操作步骤为:abdcfe;
故答案为:abdcfe;
③配制100mL4.0mol•L-1NaOH溶液,需要氢氧化钠的质量m=0.1L×4.0mol/L×40g/mol=16.0g;
故答案为:16.0;
④A.没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故A不选;
B.如果加水超过了刻度线,取出水使液面恰好到刻度线,导致溶质的物质的量偏小,溶液浓度偏低,故B不选;
C.容量瓶没有干燥,对溶质的物质的量和溶液体积的不产生影响,溶液浓度不准确,故C选;
故选:C.
点评 本题考查了元素化合物性质及一定物质的量浓度溶液的配制,明确氯气的性质是解题关键,题目难度不大.

①Cl2+2NaOH═NaCl+NaClO+H2O
②3Cl2+6NaOH(热)═5NaCl+NaClO3+3H2O
完全反应后得到NaCl、NaClO和NaClO3的混合溶液.经测定其中NaClO和NaClO3物质的量之比为1:2,则反应中被还原的Cl2与被氧化的Cl2的物质的量之比为( )
| A. | 11:3 | B. | 2:3 | C. | 10:3 | D. | 3:4 |
①增加反应物的浓度 ②升高温度 ③加入正催化剂 ④增大压强 ⑤将固体块状粉碎成粉末状.
| A. | ①②③④ | B. | ①②③⑤ | C. | ①②③ | D. | ②③④ |
| A. | BeCl2 | B. | BF3 | C. | CCl4 | D. | H2O |
| A. | 用品红溶液鉴别CO2和SO2 | |
| B. | 用湿润的pH试纸测稀碱液的pH | |
| C. | 用NaOH溶液液鉴别MgCl2和AlCl3溶液 | |
| D. | 用焰色反应鉴别NaCl和KCl |
| A. | 沸点不同的液体可用蒸馏的方法分离 | |
| B. | 易溶与难溶的固体混合物可用溶解、过滤、蒸发、结晶的方法分离 | |
| C. | 用酒精可以从碘水中萃取碘 | |
| D. | 汽油和水的化合物不可以用分液漏斗分离 |
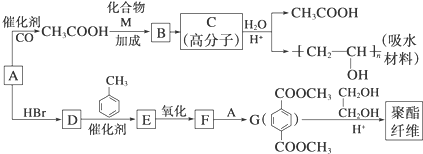
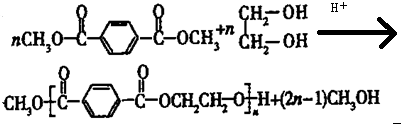 .
.