题目内容
8.下列物质的水溶液中存在溶质分子的是( )| A. | HCl | B. | NaHCO3 | C. | 蔗糖 | D. | Na2CO3 |
分析 非电解质、弱电解质溶于水时在水溶液中存在溶质分子,据此分析解答.
解答 解:A.HCl是强电解质,在水溶液中完全电离生成阴阳离子,则溶液中不存在溶质分子,故A不选;
B.碳酸氢钠是强电解质,在水溶液中完全电离生成阴阳离子,则溶液中不存在溶质分子,故B不选;
C.蔗糖是非电解质,在水溶液中以分子存在,所以其水溶液中存在溶质分子,故C选;
D.碳酸钠是可溶性强电解质,在水溶液中完全电离生成阴阳离子,则溶液中不存在溶质分子,故D不选;
故选C.
点评 本题考查电解质的电离,为高频考点,明确电解质和非电解质概念内涵及其区别、强弱电解质概念及其区别是解本题关键,注意碳酸氢钠在水溶液中完全电离生成金属阳离子和酸式酸根离子离子,题目难度不大.

练习册系列答案
相关题目
3.铁有δ、γ、α三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化.下列说法不正确的是( )
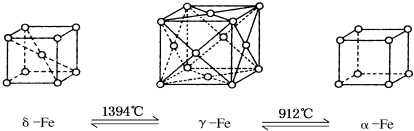

| A. | 将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体类型相同 | |
| B. | α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个 | |
| C. | 若δ-Fe晶胞边长为a cm,α-Fe晶胞边长为b cm,则两种晶体密度比为2b3:a3 | |
| D. | δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个 |
13.0.05mol/L某金属氯化物20mL,恰好与20mL0.1mol/L的AgNO3溶液反应,则该金属氯化物的化学式可表示为( )
| A. | XCl | B. | XCl2 | C. | XCl3 | D. | XCl4 |
20.已知:
Fe2O3(s)+$\frac{3}{2}$C(s)═$\frac{3}{2}$CO2(g)+2Fe(s);△H=234.1KJ/mol
C(s)+O2(g)═CO2(g);△H=-393.5KJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的△H是( )
Fe2O3(s)+$\frac{3}{2}$C(s)═$\frac{3}{2}$CO2(g)+2Fe(s);△H=234.1KJ/mol
C(s)+O2(g)═CO2(g);△H=-393.5KJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的△H是( )
| A. | -1648.8KJ/mol | B. | -824.4KJ/mol | C. | +1648.8KJ/mol | D. | -744.7KJ/mol |
18.下列能级符号表示错误的是( )
| A. | 2p | B. | 4d | C. | 5s | D. | 3f |
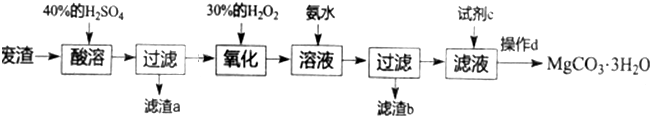
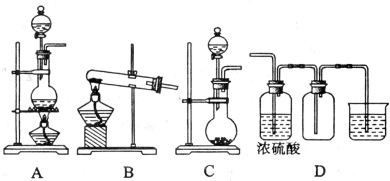
 ;
; ;A、B、E形成的化合物
;A、B、E形成的化合物 ;D、E形成的化合物
;D、E形成的化合物 .
.