��Ŀ����
 ú��Һ���ǰѹ���ú̿ͨ����ѧ�ӹ����̣�ʹ��ת����ΪҺ��ȼ�ϡ�����ԭ�ϺͲ�Ʒ���Ƚ��ྻú������
ú��Һ���ǰѹ���ú̿ͨ����ѧ�ӹ����̣�ʹ��ת����ΪҺ��ȼ�ϡ�����ԭ�ϺͲ�Ʒ���Ƚ��ྻú��������1����2L���ܱ������У���CO2��H2�ϳɼ״�CO2��g��+3H2��g���TCH3OH��g��+H2O��g�����������������������£�̽���¶ȶԷ�Ӧ��Ӱ�죬ʵ������ͼ��ʾ��ע��T2��T1������300�棩��
���¶�ΪT2ʱ���ӷ�Ӧ��ʼ��ƽ�⣬���ɼ״���ƽ����Ӧ����Ϊ
��ͨ������ͼ�����Եó��¶ȶԷ�ӦCO2��g��+3H2��g���TCH3OH��g��+H2O��g����Ӱ����Ը���Ϊ
������������˵��������Ӧ�Ѵﵽƽ��״̬����
a����ϵѹǿ���ֲ���
b���ܱ�������CO2��H2��CH3OH��g����H2O��g��4�����干��
c��CH3OH��H2���ʵ���֮��Ϊ1��3
d��ÿ����1mol CO2��ͬʱ����3molH2
��2����һ���¶��½�3mol CO2��2mol H2�����2L���ܱ������У��������·�Ӧ��
CO2��g��+H2��g��?CO��g��+H2O��g��
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
����֪��700��ʱ���÷�Ӧ��ƽ�ⳣ��K1=0.6������¶��·�ӦCO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K2=
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
����֪��1 000��ʱ���÷�Ӧ��ƽ�ⳣ��K4Ϊ1.0����÷�ӦΪ
����1 000���£�ijʱ��CO2�����ʵ���Ϊ2.0mol�����ʱv��
���㣺���ʵ�����Ũ����ʱ��ı仯����,�û�ѧƽ�ⳣ�����м���,��ѧƽ��״̬���ж�,��ѧƽ��ļ���
ר�⣺
��������1���ٸ��ݷ�Ӧ����v=
�����㼴�ɣ�
���¶��ܼӿ컯ѧ��Ӧ���ʣ���ʹ��ѧƽ���������ȷ�����У�
�۸��ݻ�ѧƽ��״̬���������桢���������䡢�����ش��жϣ�
��2���ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
��
�ڷ�ӦCO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K2=
��
��Ӧ
CO2��g��+
H2��g��?
CO��g��+
H2O��g����ƽ�ⳣ��K3=
��
�������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���
�ܸ���Ũ������ƽ�ⳣ���жϷ�Ӧ������ƽ�ⳣ�����㷴Ӧ�Ķ�����̼�������ٽ��ת���ʼ��������̼��ת���ʣ�
| ��c |
| ��t |
���¶��ܼӿ컯ѧ��Ӧ���ʣ���ʹ��ѧƽ���������ȷ�����У�
�۸��ݻ�ѧƽ��״̬���������桢���������䡢�����ش��жϣ�
��2���ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
�ڷ�ӦCO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K2=
| c(CO2)c(H2) |
| c(CO)c(H2O) |
��Ӧ
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| K1 |
�������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���
�ܸ���Ũ������ƽ�ⳣ���жϷ�Ӧ������ƽ�ⳣ�����㷴Ӧ�Ķ�����̼�������ٽ��ת���ʼ��������̼��ת���ʣ�
���
�⣺��1�����¶�ΪT2ʱ���ӷ�Ӧ��ʼ��ƽ�⣬���ɼ״���ƽ����Ӧ����v=
=
=
mol/��L?min�����ʴ�Ϊ��
mol/��L?min����
���¶��ܼӿ컯ѧ��Ӧ���ʣ���ʹ��ѧƽ���������ȷ�����У�T2��T1������ͼһ���¶����ߣ��״������ʵ�����С������ƽ�������ƶ��������Ե���������һ��ʱ�����ڸû�ѧ��Ӧ��CO2��g��+3H2��g��=CH3OH��l��+H2O��l���������¶ȣ���Ӧ���ʼӿ죻����������һ��ʱ�������¶ȣ�ƽ�������ƶ���
�ʴ�Ϊ������������һ��ʱ�������¶ȣ���Ӧ���ʼӿ죻����������һ��ʱ�������¶ȣ�ƽ�������ƶ���
��a���÷�Ӧ��һ����Ӧǰ������ϵ���ͱ仯�ķ�Ӧ������ϵѹǿ���ֲ��䣬֤���ﵽƽ�⣬��a��ȷ��
b���ܱ�������CO2��H2��CH3OH��g����H2O��g��4�����干�棬ֻ��֤����һ�����淴Ӧ������֤����ƽ��״̬����b����
c��CH3OH��H2���ʵ���֮��Ϊ1��3������֤����ƽ��״̬����c����
d��ÿ����1mol CO2��ͬʱ����3molH2����֤�����淴Ӧ������ȣ���d��ȷ��
�ʴ�Ϊ��ad��
��2����CO2��g��+H2��g��?CO��g��+H2O��g��
��Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
���ʴ�Ϊ��
��
�ڷ�ӦCO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K2=
=
=
=1.67��
��Ӧ
CO2��g��+
H2��g��?
CO��g��+
H2O��g����ƽ�ⳣ��K3=
=
��
�ʴ�Ϊ��1.67��
��
����1 000��ʱ���÷�Ӧ��ƽ�ⳣ��K4Ϊ1.0�������¶�ƽ�ⳣ������ƽ��������Ӧ�����ƶ���˵������Ӧ�����ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��CO2��g��+H2��g���TCO��g��+H2O��g��
��ʼ1.5 1 0 0
��Ӧ0.5 0.5 0.5 0.5
ƽ��1 0.5 0.5 0.5
Ũ����=
=0.5��1����Ӧ������Ӧ�����ƶ�������v��������v���棩��
3mol CO2��2mol H2�����2L���ܱ������У��������̼����������ʼŨ�ȷֱ�Ϊ1.5mol/L��1mol/L����1 000���£�ijʱ��CO2�����ʵ���Ϊ2.0mol��ijʱ�̶�����̼��Ũ����1mol/L��
����¶��´ﵽƽ��ʱ����Ӧ�Ķ�����̼�����ʵ���Ũ��Ϊx
CO2��g��+H2��g���TCO��g��+H2O��g��
��ʼ1.5 1 0 0
��Ӧx x x x
ƽ��1.5-x 1-x x x
=1.0��x=0.6
������̼��ת����=
��100%=40%��
�ʴ�Ϊ������40%��
| ��c |
| ��t |
| ||
| tBmin |
| nB |
| 2tB |
| nB |
| 2tB |
���¶��ܼӿ컯ѧ��Ӧ���ʣ���ʹ��ѧƽ���������ȷ�����У�T2��T1������ͼһ���¶����ߣ��״������ʵ�����С������ƽ�������ƶ��������Ե���������һ��ʱ�����ڸû�ѧ��Ӧ��CO2��g��+3H2��g��=CH3OH��l��+H2O��l���������¶ȣ���Ӧ���ʼӿ죻����������һ��ʱ�������¶ȣ�ƽ�������ƶ���
�ʴ�Ϊ������������һ��ʱ�������¶ȣ���Ӧ���ʼӿ죻����������һ��ʱ�������¶ȣ�ƽ�������ƶ���
��a���÷�Ӧ��һ����Ӧǰ������ϵ���ͱ仯�ķ�Ӧ������ϵѹǿ���ֲ��䣬֤���ﵽƽ�⣬��a��ȷ��
b���ܱ�������CO2��H2��CH3OH��g����H2O��g��4�����干�棬ֻ��֤����һ�����淴Ӧ������֤����ƽ��״̬����b����
c��CH3OH��H2���ʵ���֮��Ϊ1��3������֤����ƽ��״̬����c����
d��ÿ����1mol CO2��ͬʱ����3molH2����֤�����淴Ӧ������ȣ���d��ȷ��
�ʴ�Ϊ��ad��
��2����CO2��g��+H2��g��?CO��g��+H2O��g��
��Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
�ڷ�ӦCO��g��+H2O��g��?CO2��g��+H2��g����ƽ�ⳣ��K2=
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| 1 |
| K1 |
| 1 |
| 0.6 |
��Ӧ
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| K1 |
| 0.6 |
�ʴ�Ϊ��1.67��
| 0.6 |
����1 000��ʱ���÷�Ӧ��ƽ�ⳣ��K4Ϊ1.0�������¶�ƽ�ⳣ������ƽ��������Ӧ�����ƶ���˵������Ӧ�����ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��CO2��g��+H2��g���TCO��g��+H2O��g��
��ʼ1.5 1 0 0
��Ӧ0.5 0.5 0.5 0.5
ƽ��1 0.5 0.5 0.5
Ũ����=
| 0��52 |
| 1��0.5 |
3mol CO2��2mol H2�����2L���ܱ������У��������̼����������ʼŨ�ȷֱ�Ϊ1.5mol/L��1mol/L����1 000���£�ijʱ��CO2�����ʵ���Ϊ2.0mol��ijʱ�̶�����̼��Ũ����1mol/L��
����¶��´ﵽƽ��ʱ����Ӧ�Ķ�����̼�����ʵ���Ũ��Ϊx
CO2��g��+H2��g���TCO��g��+H2O��g��
��ʼ1.5 1 0 0
��Ӧx x x x
ƽ��1.5-x 1-x x x
| x2 |
| (1.5-x)(1-x) |
������̼��ת����=
| 0.6mol/L |
| 1.5mol/L |
�ʴ�Ϊ������40%��
����������Ŀ�ۺϿ���ѧ���Ի�ѧƽ���ƶ���Ӱ�졢��ѧƽ��״̬���жϡ��Լ���ѧƽ��ļ���֪ʶ�������ۺ�֪ʶ�Ŀ��飬�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
�����й�ԭ�ӽṹ��Ԫ�����ʵ�˵����ȷ���ǣ�������
| A��Si��P��S��ClԪ�صĵ�������������Խ��Խ���� |
| B��Ԫ��ԭ������������Խ�࣬Ԫ�ؽ�����Խǿ |
| C��Ԫ�����ڱ�����18�У���3���ǵڢ�B�壬��17���ǵڢ�A�� |
| D��F-��O2-��Mg2+��Na+���Ӱ뾶��С |
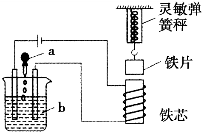 ��ͼ��ʾ�����ձ��ڵ���Һb��������Һaʱ���������ɳӵĶ�������СȻ��Ȼ�����������Һa��b�ֱ��ǣ�������
��ͼ��ʾ�����ձ��ڵ���Һb��������Һaʱ���������ɳӵĶ�������СȻ��Ȼ�����������Һa��b�ֱ��ǣ�������| A��NaOH��H2SO4 |
| B��BaCl2��NaOH |
| C��Ba��OH��2��Na2SO4 |
| D��NH3?H2O��CH3COOH |
���ȵ�¯�����з�Ӧ��C��s��+O2��g��=CO2��g����H=-392kJ/mol����¯����ͨ��ˮ����ʱ�������·�Ӧ��C��s��+H2O��g��=CO��g��+H2��g����H=+131kJ/mol��CO��g��+
O2��g��=CO2��g����H=-282kJ��H2��g��+
O2��g��=H2O��g����H=-241kJ/mol�������Ϸ�Ӧ�ƶ������ȵ�¯����ͨ��ˮ����ʱ��������
| 1 |
| 2 |
| 1 |
| 2 |
| A�����ܽ�ʡȼ�ϣ�����ʹ¯��˲����� |
| B���䲻��ʹ¯������������Խ�ʡȼ�� |
| C������ʹ¯����������ܽ�ʡȼ�� |
| D���Ȳ���ʹ¯��������ֲ��ܽ�ʡȼ�� |
��ͼ��Ԫ�����ڱ������ڵ�һ���֣�����Fԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+1������������Ϊ2n2-1������˵������ȷ���ǣ�������
| A | B | C | |
| D | E | F |
| A��D�ĵ����dz����İ뵼����� |
| B��B��E�γɵĻ����ﲻֻһ�� |
| C��C��F��ԭ������֮��һ��Ϊ8 |
| D��A������������ˮ�����ܺ�Al2O3��Ӧ |
 �����£���0.1mol/LHCl�ζ�10mL0.1mol/LNa2CO3���ζ�������ͼ��ʾ������˵����ȷ���ǣ�������
�����£���0.1mol/LHCl�ζ�10mL0.1mol/LNa2CO3���ζ�������ͼ��ʾ������˵����ȷ���ǣ�������| A��ˮ����̶��ɴ�С��˳��Ϊ��a��b��c��d |
| B��a��ʱ��c��Na+����c��CO32-����c��HCO3-����c��OH-�� |
| C��b��ʱ��3c��Na+��=2c��CO32-��+2c��HCO3-��+2c��H2CO3�� |
| D��d��ʱ��c��H+����c��HCO3-��=c��CO32-�� |
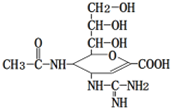 ������H7N9�����������ѹ��ɡ����й���Ӱ��Ĺ�������������̬������֪������Τ�����в�������ø���Ƽ���������в�����������������ϵķ�ʽ���еģ����и߶������ԣ�����ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������
������H7N9�����������ѹ��ɡ����й���Ӱ��Ĺ�������������̬������֪������Τ�����в�������ø���Ƽ���������в�����������������ϵķ�ʽ���еģ����и߶������ԣ�����ӽṹ��ͼ��ʾ������˵����ȷ���ǣ�������| A�������ʵķ���ʽΪC12H19N4O7 |
| B��1mol��������NaOH��Һ��Ӧ����������4molNaOH |
| C����һ�������£������ʿ��Է�����ȥ���ӳɡ�ȡ���ȷ�Ӧ |
| D����������ʹ��ˮ����������Һ��ɫ������FeCl3��Һ������ɫ��Ӧ |