题目内容
8.充分燃烧一种只含C、H、O三种元素的有机物,它们消耗O2和生成CO2的体积比都为5:4.(l)此类中相对分子质量最小的有机物的结构简式为CH3CHO;
(2)这类有机物充分燃烧时,生成的CO2和H2O的物质的量之比为1:1.且能发生水解反应的有机物的结构有4种.
分析 (1)设有机物的通式为CxHyOz,则与O2燃烧的方程式为CxHyOz+(x+$\frac{y}{4}$-$\frac{z}{2}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,据此进行分析;
(2)由(1)得,y=2z+x①,生成的CO2和H2O的物质的量之比为1:1,则x:$\frac{y}{2}$=1:1,则y=2x②,联立①②2z=x,y=2x(x,y,z为整数),且能发生水解反应,故有机物有羧基或者酯基,故有机物含2个O,即z=2,则x=4,y=8,故有机物的分子式为C4H8O2,据此确定可能的结构.
解答 解:(1)设有机物的通式为CxHyOz,
则与O2燃烧的方程式为CxHyOz+(x+$\frac{y}{4}$-$\frac{z}{2}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,它们消耗O2和生成CO2的体积比都为5:4,则(x+$\frac{y}{4}$-$\frac{z}{2}$):x=5:4,整理得y=2z+x,且x,y,z为整数,要得到相对分子质量最小的有机物,故x=2,y=4,z=1,故有机物分子式为C2H4O,结构简式为CH3CHO,
故答案为:CH3CHO;
(2)由(1)得,y=2z+x①,生成的CO2和H2O的物质的量之比为1:1,则x:$\frac{y}{2}$=1:1,则y=2x②,联立①②2z=x,y=2x(x,y,z为整数),且能发生水解反应,故有机物有羧基或者酯基,故有机物含2个O,即z=2,则x=4,y=8,故有机物的分子式为C4H8O2,故能发生水解反应的有机物的结构有
HOOCH2CH2CH3,HOOCH(CH3)2,CH3COOCH2CH3,CH3CH2COOCH3,故有4种结构,
故答案为:4.
点评 本题考查考查了有机物分子式确定的计算,题目难度中等,关键根据消耗的氧气和生成的二氧化碳的体积比是5:4,确定机物分子组成可表示为CxHyOz,试题培养了学生的分析能力及化学计算能力.

①第一份加过量NaOH溶液后加热,收集到0.01mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到11.65g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
| A. | 由①可知原溶液存在离子为NH4+,其浓度为0.01mol/L | |
| B. | 原溶液一定存在Cl- | |
| C. | 原溶液肯定没有Fe3+、Mg2+,一定含有Na+ | |
| D. | n(NH4+):n(Al3+):n(SO42-)=1:1:5 |
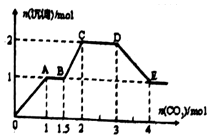 现有易溶强电解质的混合溶液10L,共中可能含K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与遇入CO2的量之问的关系如图所示,下列说法正确的是( )
现有易溶强电解质的混合溶液10L,共中可能含K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与遇入CO2的量之问的关系如图所示,下列说法正确的是( )| A. | 该溶液中能确定存在的离子是Ba2+、Na+、Cl-、NH4+ | |
| B. | 肯定不存在的离子是Cl-、OH- | |
| C. | 若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为:0.2mol/L | |
| D. | OA段反应的离子方程式::2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
 如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )
如图是NaCl晶体的一个晶胞结构棋型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替.则下列关于KO2晶体结构的叙述中正确的是( )| A. | 与K+距离相等且最近的O2-有8个 | |
| B. | 与K+距离相等且最近的O2-构成的多面体是六面体 | |
| C. | 一个KO2晶胞中的K+和O2-的粒子数都是4个 | |
| D. | 与K+距离相等且最近的K+有8个 |
(1)分解海水时,实现了从太阳能转变为化学能.生成的氢气用于燃料电池时,实现化学能转变为电能.
通常把拆开1mol 某化学键所吸收的能量或形成1mol某化学键所放出的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,化学反应的反应热等于反应中断裂旧化学键的之和与反应中形成新化学键的键能之和的差.
| 化学键 | H-H | N≡N | N-H |
| 键能/KJ•mol-1 | 436 | 946 | 390.8 |
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
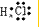 ②⑤
②⑤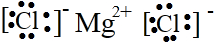 ③⑦
③⑦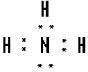
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
| A. | 34S原子核内中子数为18 | B. | 2H+的酸性比1H+的酸性更强 | ||
| C. | 16O与18O的化学性质几乎完全相同 | D. | 13C和15N原子核内的质子数相差1 |
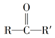 (R、R′为烃基)结构的分子
(R、R′为烃基)结构的分子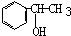 ;
;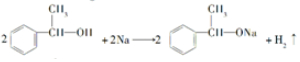 ;
;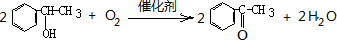 .
.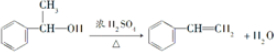 .脱水后的产物,发生聚合反应的化学方程式
.脱水后的产物,发生聚合反应的化学方程式 .
.