题目内容
草酸晶体的组成可表示为:H2C2O4?XH2O,为测定X值,进行下列实验:
①称取wg草酸晶体配成100.0mL水溶液;
②取25.00mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为
c mol?L-1KMnO4溶液滴定.滴定时,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)若滴定时,反应前后的两次读数分别为a和b,则实验测得所配草酸溶液的物质的量浓度为 ,由此计算出草酸晶体的X值是 .
(2)假设滴定终点时,用去VmL KMnO4溶液,则待测草酸的物质的量浓度为 mol?L-1.
①称取wg草酸晶体配成100.0mL水溶液;
②取25.00mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为
c mol?L-1KMnO4溶液滴定.滴定时,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)若滴定时,反应前后的两次读数分别为a和b,则实验测得所配草酸溶液的物质的量浓度为
(2)假设滴定终点时,用去VmL KMnO4溶液,则待测草酸的物质的量浓度为
考点:化学方程式的有关计算,中和滴定
专题:计算题
分析:(1)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,根据关系式2KMnO4~5H2C2O4计算25.0mL草酸溶液中n(H2C2O4),进而计算100mL草酸溶液中n′(H2C2O4)和c(H2C2O4),计算草酸的质量,根据化学式质量分数计算求X的值;
(2)根据高锰酸钾和草酸之间的关系式进行解答.
(2)根据高锰酸钾和草酸之间的关系式进行解答.
解答:
解:(1)滴定管的刻度由上而下刻度增大,滴定前后两次读数分别为amL和bmL,故消耗KMnO4溶液体积(b-a)mL,n(KMnO4)=c mol?L-1×(b-a)×10-3L=c×(b-a)×10-3mol,根据关系式2KMnO4~5H2C2O4可知25.0mL草酸溶液中n(H2C2O4)=2.5×c×(b-a)×10-3mol,进而计算100mL草酸溶液中n′(H2C2O4)=2.5×c×(b-a)×10-3mol×
=c×(b-a)×10-2mol,c(H2C2O4)=
=
c×(b-a)mol/L;
草酸晶体中草酸的质量为c×(b-a)×10-2mol×90g/mol=0.9c(b-a)g,由化学式可知:
=
,解得x=
-5,
故答案为:
c(b-a)mol/L;
-5;
(2)根据2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O知,草酸的物质的量浓度=
=0.1CVmol/L,
故答案为:0.1CV.
| 100mL |
| 25mL |
| c×(b-a)×10-2mol |
| 0.1L |
| 1 |
| 10 |
草酸晶体中草酸的质量为c×(b-a)×10-2mol×90g/mol=0.9c(b-a)g,由化学式可知:
| 90 |
| 90+18x |
| c×(b-a)×10-2mol×90g/mol |
| Wg |
| 50W |
| 9c(b-a) |
故答案为:
| 1 |
| 10 |
| 50W |
| 9c(b-a) |
(2)根据2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O知,草酸的物质的量浓度=
Cmol/L×10-3VL×
| ||
| 0.025L |
故答案为:0.1CV.
点评:本题考查滴定应用与计算,难度中等,注意滴定中经常根据关系式进行计算,掌握根据关系式计算方法.

练习册系列答案
相关题目
下列体系加压后,对化学反应速率没有影响的是( )
| A、2SO2+O2?2SO3 |
| B、CO+H2O(g)?CO2+H2 |
| C、CO2+H2O?H2CO3 |
| D、H++OH-?H2O |
下列反应属于氧化还原反应的是( )
| A、CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| B、SO2+H2O=H2SO3 |
| C、Cl2+2NaOH=NaCl+NaClO+H2O |
| D、NaBr+AgNO3=AgBr↓+NaNO3 |
下列不属于金属的通性的是( )
| A、导电导热性 | B、延展性 |
| C、有光泽 | D、熔点很高 |
在保持平衡的天平的左右两盘中各放一只大小和质量均相同的烧杯,两烧杯中都盛有1mol?L-1的稀硫酸100mL,然后分别向两烧杯中加入一定质量的金属,充分反应后天平仍保持平衡,则金属的质量分别是( )
| A、4.6g Na 4.8g Mg |
| B、5g Na 5g Al |
| C、2.3g Na 2.4g Mg |
| D、1.8g Al 2.4g Mg |
下列有关说法正确的是( )
| A、盐酸可以导电,所以盐酸是电解质 |
| B、氧化还原反应中都只有一种元素化合价升高 |
| C、纳米材料也是一种胶体 |
| D、丁达尔效应,是胶体粒子对光散射形成的 |
某粒子的结构示意图为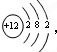 ,关于该粒子的说法不正确的是( )
,关于该粒子的说法不正确的是( )
 ,关于该粒子的说法不正确的是( )
,关于该粒子的说法不正确的是( )| A、属于金属离子 |
| B、核外有三个电子层 |
| C、核电荷数为12 |
| D、在化学反应中溶液失去2个电子 |
在K2CO3样品中含Na2CO3、KNO3、Ba(NO3)2中的一或二种杂质,将13.8g样品溶于足量水中得到澄清溶液,再加入过量CaCl2溶液,可得9.0g沉淀,则原样品中含有的杂质会是( )
| A、肯定有Na2CO3,没有Ba(NO3)2 |
| B、肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3 |
| C、肯定没有Na2CO3,Ba(NO3)2 |
| D、无法判断何种为肯定或否定的杂质 |