题目内容
2.如图1所示,A是恒容的密闭容器,B是一个体积可变的充气气囊.保持恒温,关闭K2,将1molN2和3molH2通过K3充入B中,将2molN2和6molH2通过K1充入A中;起始时A、B的体积相同均为aL,达到平衡时,V(B)=0.8aL,①图2示意图中正确,且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是d.
②A、B中N2转化率的关系:α(A)<α(B)(填“>”、“<”或“=”);
③打开K2,一段时间又达到平衡时,B的体积为1.4aL(连通管中气体体积不计)
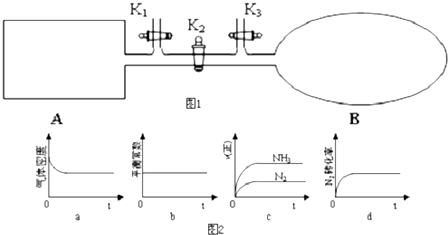
分析 ①可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
②随反应进行混合气体物质的量减小,A是恒温恒容,B是恒温恒压,故平衡时A的压强比B中的小,B等效为在A中平衡基础上增大压强,平衡正向移动;
③打开K2,一段时间又达到平衡时,等效为开始通入3molN2和9molH2再恒温恒容到达的平衡,与B中平衡为等效平衡,平衡时同种物质的转化率相等,则平衡时混合气体物质的量为B中平衡时的3倍,根据恒温恒压下体积之比等于物质的量之比计算平衡时气体体积,减去A容器体积即为B的体积.
解答 解:①a.混合气体总质量一定,容器A的容积不变,故密度数值不变,所以不能说明反应达到平衡状态,故a错误;
b.恒温条件下,平衡常数保持不变,则不能说明反应达到平衡状态,故b错误;
c.随反应进行氮气速率减小、氨气速率增大,图象中速率变化不符合,故c错误;
d.N2的转化率先增大,后保持不变,说明反应达到平衡状态,故d正确;
故答案为:d;
②随反应进行混合气体物质的量减小,A是恒温恒容,B是恒温恒压,故平衡时A的压强比B中的小,B等效为在A中平衡基础上增大压强,平衡正向移动,则N2转化率的关系:α(A)<α(B),
故答案为:<;
③打开K2,一段时间又达到平衡时,等效为开始通入3molN2和9molH2再恒温恒容到达的平衡,与B中平衡为等效平衡,平衡时同种物质的转化率相等,则平衡时混合气体物质的量为B中平衡时的3倍,恒温恒压下体积之比等于物质的量之比,故平衡时气体体积为0.8a L×3=2.4a L,则B的体积为2.4a L-aL=1.4a L,
故答案为:1.4a L.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、化学平衡图象,③中关键是对等效平衡规律的理解掌握.

 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案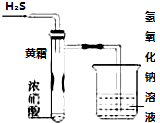 某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是
某同学用下列实验装置探究硝酸的性质.根据图示判断下列结论不正确的是( )
| A. | 试管内壁上“黄霜”的成分是硫 | |
| B. | 该实验探究说明浓硝酸既有氧化性,又有挥发性 | |
| C. | 烧杯内的NaOH溶液的作用是除去尾气,防止尾气污染环境 | |
| D. | H2S用SO2代替,将无明显反应现象 |
| A. | 水解平衡正向移动 | B. | 各微粒浓度均变小 | ||
| C. | 溶液中离子数目增多 | D. | c(Al3+)与c(SO42-)的比值减小 |
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. |  | ||
| C. |  | D. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
| A. | ④>③>②>① | B. | ③>④>②>① | C. | ②>③>④>① | D. | ③>②>④>① |
| A. | 打开啤酒瓶盖,产生大量气泡 | |
| B. | 稀释CH3COOH时,溶液中CH3COO-数目增多 | |
| C. | 工业合成氨常用500℃左右的温度 | |
| D. | 热的纯碱溶液的去污效果比冷的好 |
 27H2O↑+10M+aAl2O3下列说法正确的是
27H2O↑+10M+aAl2O3下列说法正确的是