题目内容
11.下列化学反应中观察不到颜色变化的是( )| A. | 往品红溶液中通入SO2 | B. | NO中混入空气 | ||
| C. | 往氨水中滴加酚酞 | D. | 往Ba(OH)2溶液中滴加盐酸 |
分析 A.二氧化硫具有漂白性;
B.一氧化氮与氧气反应生成二氧化氮;
C.酚酞遇到碱显红色;
D.氢氧化钡与盐酸反应生成氯化钡和水.
解答 解:A.二氧化硫具有漂白性,能够使品红溶液褪色,故A正确;
B.一氧化氮与氧气反应生成二氧化氮,由无色变为红棕色,故B正确;
C.氨水为弱碱,显碱性,加入酚酞变为红色,故C正确;
D.氢氧化钡与盐酸反应生成氯化钡和水,无明显现象,故D错误;
故选:D.
点评 本题考查了元素化合物知识,明确二氧化硫、一氧化氮、一水合氨的性质是解题关键,题目难度不大.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
6.黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)Na2SO3+H2O2=Na2SO4+H2O.
H2O2可以看作是一种很弱的酸,写出其电离方程式:H2O2?H++HO2-.
(3)该黄铁矿石中硫元素的质量分数为$\frac{32m{\;}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=0.5000mol/L.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)Na2SO3+H2O2=Na2SO4+H2O.
H2O2可以看作是一种很弱的酸,写出其电离方程式:H2O2?H++HO2-.
(3)该黄铁矿石中硫元素的质量分数为$\frac{32m{\;}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
2.物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
| A. | Ba(OH)2、Na2S03、FeCl3、KCl | B. | Na2Si03、Na2C03、KN03、NH4Cl | ||
| C. | NH3、H20、H3P04、Na2S04、H2S04 | D. | HCl、CH2COOH、C2H5OH、Na2SiO3 |
19.在强酸性溶液中能大量共存的透明离子组是( )
| A. | K+ Na+ NO3- CO32- | B. | Na十 Fe3+ SCN- SO42- | ||
| C. | K+ Na十 Cl- AlO2- | D. | Al3+ Na+ Cl- SO42- |
16. 五种短周期元素的部分性质数据如下:
五种短周期元素的部分性质数据如下:
(1)Z离子的结构示意图为 .
.
(2)关于Y、Z两种元素,下列叙述正确的是b(填序号)
a.简单离子的半径Y>Z b.气态氢化物的稳定性Y比Z强
c.最高价氧化物对应的水化物的酸性Z比Y强
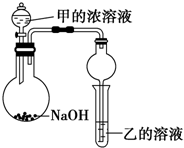
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.
某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是把浓氨水滴到NaOH固体上,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O?NH3•H2O?NH4++OH-向左移动,且过程中放热,故有利于NH3放出.一段时间后,观察到试管中的现象是生成白色沉淀,发生反应的离子方程式是3NH3.H2O+Al3+=Al(OH)3↓+3NH4+.
(4)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为+3.
 五种短周期元素的部分性质数据如下:
五种短周期元素的部分性质数据如下:| 元素 | T | X | Y | Z | W |
| 原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
 .
.(2)关于Y、Z两种元素,下列叙述正确的是b(填序号)
a.简单离子的半径Y>Z b.气态氢化物的稳定性Y比Z强
c.最高价氧化物对应的水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.
某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是把浓氨水滴到NaOH固体上,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O?NH3•H2O?NH4++OH-向左移动,且过程中放热,故有利于NH3放出.一段时间后,观察到试管中的现象是生成白色沉淀,发生反应的离子方程式是3NH3.H2O+Al3+=Al(OH)3↓+3NH4+.
(4)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为+3.
3. 已知25℃时有关弱酸的电离平衡常数:
已知25℃时有关弱酸的电离平衡常数:
(1)同温度下,等pH值的a.NaHCO3 b.NaCN c.Na2CO3溶液的物质的量浓度由大到小的顺序为a>b>c(填序号).
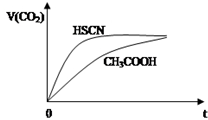
(2)25℃时,将20mL 0.1mol•L-1CH3COOH溶液和20mL 0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:相同温度下HSCN比CH3COOH的电离平衡常数大,同浓度时电离出的氢离子浓度大,与NaHCO3溶液反应快.反应结束后所得两溶液中,c(SCN-)>c(CH3COO-)(填“>”、“<”或“=”)
(3)若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号)
a.c(CH3COO-) b.c(H+) c.KW d.醋酸电离平衡常数.
 已知25℃时有关弱酸的电离平衡常数:
已知25℃时有关弱酸的电离平衡常数:| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
(2)25℃时,将20mL 0.1mol•L-1CH3COOH溶液和20mL 0.1mol•L-1HSCN溶液分别与20mL 0.1mol•L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:相同温度下HSCN比CH3COOH的电离平衡常数大,同浓度时电离出的氢离子浓度大,与NaHCO3溶液反应快.反应结束后所得两溶液中,c(SCN-)>c(CH3COO-)(填“>”、“<”或“=”)
(3)若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是b(填序号)
a.c(CH3COO-) b.c(H+) c.KW d.醋酸电离平衡常数.
20.在Na2O2与水反应中,叙述正确的是( )
| A. | O2是还原产物 | |
| B. | NaOH是氧化产物 | |
| C. | Na2O2中,-1价的氧既得电子,又失电子 | |
| D. | Na2O2是氧化剂,水是还原剂 |
1.下列说法错误的是( )
| A. | 为使水果保鲜,可在水果箱内放入高锰酸钾溶液浸泡过的硅藻土 | |
| B. | PM2.5表面积大,能吸附大量的有毒、有害物质 | |
| C. | 高纯硅在太阳能电池及信息高速传输中有重要应用 | |
| D. | 从海水中提取物质不一定要通过化学反应实现 |

