题目内容
N2O5是一种新型绿色硝化剂,其性质和制备受到人们的关注.已知一定条件下会发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0,平衡常数为K.下列叙述正确的是( )
| A、上述反应的平衡常数随温度升高而增大 |
| B、上述反应达到平衡后,只增大氧气浓度,因为K值变大了,所以平衡将向左移动 |
C、N2O5与苯发生硝化反应除了生成硝基苯(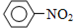 ),还有氧气生成 ),还有氧气生成 |
| D、以N2O4等为原料采用电化学方法可以合成N2O5,该合成应避免碱性环境 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、正反应吸热,升温时平衡正向移动;
B、K只受温度影响;
C、N的化合价没有发生变化,O也不会改变;
D、碱性环境中,其能够与碱反应.
B、K只受温度影响;
C、N的化合价没有发生变化,O也不会改变;
D、碱性环境中,其能够与碱反应.
解答:
解:A、正反应吸热,升温时平衡正向移动,K增大,故A正确;
B、K只受温度影响,增大氧气浓度时,平衡常数不变,故B错误;
C、N的化合价没有发生变化,O也不会改变,所以不会生成氧气,故C错误;
D、N2O4和N2O5都会和碱反应,故D正确;
故选AD.
B、K只受温度影响,增大氧气浓度时,平衡常数不变,故B错误;
C、N的化合价没有发生变化,O也不会改变,所以不会生成氧气,故C错误;
D、N2O4和N2O5都会和碱反应,故D正确;
故选AD.
点评:本题是信息给予题,依据题给信息解答,注意平衡常数只受温度影响,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
糖类、油脂和蛋白质都是人体必需的基本营养物质,下列说法中不正确的是( )
| A、淀粉、油脂和蛋白质都能发生水解反应 |
| B、糖类、油脂和蛋白质都属于高分子化合物 |
| C、氨基酸既可以与盐酸反应,也能与NaOH反应 |
| D、采用多次盐析和溶解,可以分离提纯蛋白质 |
25℃时,下列说法中,不正确的是( )
| A、将体积均为100mL、浓度均为0.1mol/L的Ba(OH)2溶液与Na2SO4溶液混合,若混合后溶液的体积为100mL,则所得溶液的pH=13 |
| B、将等体积等浓度的醋酸与CH3COONa溶液混合,所得溶液中:c(Na+)+c(H+)═c(CH3COO-)+c(OH-) |
| C、将等体积等浓度的Na2CO3溶液与NaHCO3溶液混合,所得溶液中:2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、将等体积等浓度的Na2CO3溶液与NaOH溶液混合,所得溶液中:c(Na+)>c(OH-)>c(CO32-)>c(H+) |
下列实验操作或装置符合实验要求的是( )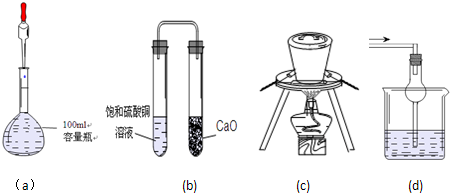

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得: