题目内容
当反应L(s)+aG(g)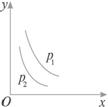
A.上述反应是放热反应 B.上述反应是吸热反应
C. a>b D. d<b
解析:分析温度与G的体积分数的变化关系。据图知,温度升高,G的体积分数降低,而G的体积分数降低,表示化学平衡向正反应方向移动,即升高温度,化学平衡向正反应方向移动。
根据化学平衡移动原理,升高温度,化学平衡向吸热反应的方向移动,则此反应的正反应为吸热反应。
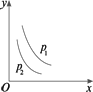
分析压强与G的体积分数的变化关系。
据图知,压强增大(p1>p2),G的体积分数也增大,而G的体积分数增大,表示化学平衡向逆反应方向移动,即增大压强,化学平衡向逆反应方向移动。
根据化学平衡移动原理,增大压强,化学平衡向气体体积缩小的方向移动,则a<b。
答案:BD

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
中学化学涉及多种常数,下列说法正确的是( )
| A、两种物质反应,不管怎样书写化学方程式,平衡常数不变 | ||
B、某温度下,2L密闭容器中加入4mol A和2mol B发生反应:3A(g)+2B(g)?4C(s)+2D( g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=
| ||
| C、温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | ||
| D、难溶电解质AB2饱和溶液中,c(A2+)=x mol?L-1,c(B-)=y mol?L-1,则Ksp值为4xy2 |