题目内容
10.下列关于 SO2 性质的说法中,不正确的是( )| A. | 能KMnO4溶液褪色 | B. | 能使品红溶液褪色 | ||
| C. | 能与 NaOH 溶液反应 | D. | 能与水反应生成硫酸 |
分析 二氧化硫为酸性氧化物,具有漂白性,为无色有刺激性气体有毒气体,具有还原性,以此解答该题.
解答 解:A.二氧化硫具有还原性,可与高锰酸钾发生氧化还原反应,故A正确;
B.二氧化硫具有漂白性,可使品红褪色,故B正确;
C.二氧化硫为酸性气体,能与 NaOH 溶液反应,故C正确;
D.二氧化硫与水反应生成亚硫酸,故D错误.
故选D.
点评 本题考查了元素化合物知识,为高频考点,侧重考查二氧化硫的性质,熟悉二氧化硫的漂白性、酸性氧化物的性质是解题关键,注意酸雨形成原因.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 工业上常用电解法制备元素C、D、E的单质 | |
| C. | 常温下,元素B、D的最高价氧化物对应的水化物之间能发生反应 | |
| D. | 化合物AE与CE具有相同类型的化学键 |
1.将金属钠投入下列物质的溶液中,有气体放出,且产生沉淀的是( )
| A. | 稀盐酸 | B. | K2SO4溶液 | C. | CuSO4溶液 | D. | NaOH溶液 |
18.下列化学用语对应正确的是( )
| A. | CH4分子的比例模型: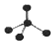 | B. | 乙酸的化学式:C2H4O2 | ||
| C. | 乙烯的结构简式CH2CH2 | D. | F-的结构示意图: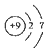 |
5.下列实验操作中正确的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球浸没在蒸馏烧瓶的液体中 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,用酒精萃取溴水中的溴 |
15.巴豆酸是一种对肠胃道有强烈刺激性、对呼吸中枢和心脏有麻痹作用的有机酸,其结构简式为CH3-CH=CH-COOH.根据巴豆酸结构特点,判断下列说法正确的是( )
| A. | 巴豆酸能使溴的CCl4溶液褪色 | |
| B. | 巴豆酸不能使酸性KMnO4溶液褪色 | |
| C. | 1mol巴豆酸能与2molH2发生加成反应 | |
| D. | 巴豆酸能与CH3CH2OH发生取代反应 |
20.如图所示,下列说法不正确的是( )
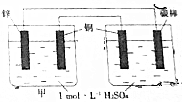

| A. | 乙池中铜电极反应是4OH--4e-═O2↑+2H2O | |
| B. | 甲池中的铜电极反应是2H++2e-═H2↑ | |
| C. | 碳棒上开始H+放电,然后是Cu2+放电 | |
| D. | 反应一段时间后甲乙两池溶液中H+的离子浓度不相同 |
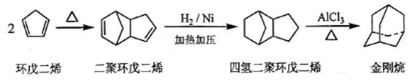
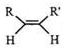 $\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO
$\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO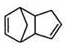 $\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$
$\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$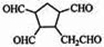 .
.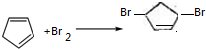 .
.