题目内容
15.下列叙述正确的是( )| A. | 1 mol氢为2 g | B. | H2O的摩尔质量为18 g | ||
| C. | 44 g CO2的体积为22.4 L | D. | 9.8 g H2SO4含0.1NA个H2SO4分子 |
分析 A.使用物质的量时,应指明具体的物质或微粒;
B、摩尔质量的单位为g/mol;
C、状况不知,气体摩尔体积不知;
D、9.8 g H2SO4的物质的量为:$\frac{9.8g}{98g/mol}$=0.1mol,结合N=nNA计算求解.
解答 解:A.使用物质的量时,应指明具体的物质或微粒,1mol氢指代不明确,不能确定为氢气还是氢原子,故A错误;
B、摩尔质量的单位为g/mol,而不是g,故B错误;
C、状况不知,气体摩尔体积不知,所以体积不知,故C错误;
D、9.8 g H2SO4的物质的量为:$\frac{9.8g}{98g/mol}$=0.1mol,N=nNA=0.1NA个H2SO4分子,故D正确;
故选D.
点评 本题考查物质的量、摩尔质量、物质的量有关计算等,比较基础,注意使用物质的量时应指明具体的物质或微粒.

练习册系列答案
相关题目
3.下列有关电池的说法不正确的是( )
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铜-锌-稀硫酸电池工作时,当转移2mol电子时,正极区可生成氢气2.24L | |
| C. | 氢氧燃料电池可把化学能转为电能 | |
| D. | 锌锰电池、镍镉电池、化学电池易造成环境污染,而氢氧燃料电池是对环境友好的电池 |
10.下列物质不属于配合物的是( )
| A. | K3[Fe(CN)6] | B. | MgCl2 | C. | [Cu(H2O)4]SO4•H2O | D. | [Ag(NH3)2]OH |
5.关于分液漏斗的使用,下列说法正确的是( )
| A. | 可在分液漏斗内用四氯化碳萃取碘酒中的碘单质 | |
| B. | 分液漏斗在使用前只需检查旋塞芯处是否漏水即可 | |
| C. | 在分液漏斗中加入萃取剂后应上下颠倒摇匀使萃取剂与溶质充分接触 | |
| D. | 放出下层液体时,应打开上方的玻璃塞,并使下端管口紧贴烧杯内壁 |
 2C.
2C.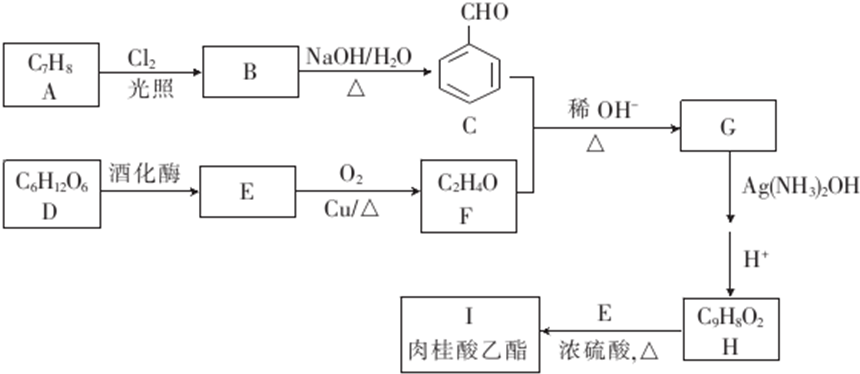
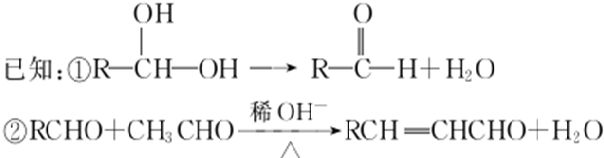
 ,E→F的反应类型是氧化反应.
,E→F的反应类型是氧化反应. .
.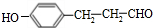 .
.