题目内容
19.已知:Kw=1.0×10-14,Al(OH)3?AlO2-+H++H2O K=2.0×10-13.则Al(OH)3溶于NaOH溶液反应的平衡常数数值为( )| A. | 10 | B. | 15 | C. | 20 | D. | 25 |
分析 由①H2O?OH-+H+、②Al(OH)3?AlO2-+H++H2O 可知,②-①得到OH-+Al(OH)3?AlO2-+H+,以此计算.
解答 解:由①H2O?OH-+H+、②Al(OH)3?AlO2-+H++H2O 可知,②-①得到OH-+Al(OH)3?AlO2-+H+,则Al(OH)3溶于NaOH溶液反应的平衡常数数值为$\frac{2.0×1{0}^{-13}}{1.0×1{0}^{-14}}$=20,故选C.
点评 本题考查化学平衡的计算,为高频考点,把握反应的关系及K的关系为解答的关键,侧重分析与计算能力的考查,注意盖斯定律的应用,题目难度不大.

练习册系列答案
相关题目
9.某学生对SO2与漂粉精的反应进行实验探究:
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)该同学推测现象1的白雾由HCl小液滴形成,并进行如下实验验证:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a的目的是检验白雾中是否含有Cl2,排除Cl2干扰.
②有同学认为由实验a、b不能判断白雾中含有HCl,理由是白雾中含有SO2,SO2可以使酸化的AgNO3溶液产生白色沉淀
(4)将A瓶中混合物过滤、洗涤,得到沉淀X.
①向沉淀X中加入稀HCl,无明显变化.取上层液体加氯化钡生成白色沉淀,则沉淀X是CaSO4
②用离子方程式解释现象4中黄绿色褪去的原因:Cl2+SO2+2H2O=4H++2Cl-+SO42-.
| 操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
 | 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀, 4.黄绿色褪去 |
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)该同学推测现象1的白雾由HCl小液滴形成,并进行如下实验验证:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀.
①实验a的目的是检验白雾中是否含有Cl2,排除Cl2干扰.
②有同学认为由实验a、b不能判断白雾中含有HCl,理由是白雾中含有SO2,SO2可以使酸化的AgNO3溶液产生白色沉淀
(4)将A瓶中混合物过滤、洗涤,得到沉淀X.
①向沉淀X中加入稀HCl,无明显变化.取上层液体加氯化钡生成白色沉淀,则沉淀X是CaSO4
②用离子方程式解释现象4中黄绿色褪去的原因:Cl2+SO2+2H2O=4H++2Cl-+SO42-.
7.除去括号内杂质所用试剂和方法不正确的是( )
| A. | Cu(Fe)----加盐酸,过滤 | B. | NaCl溶液(碘)----CCl4,萃取、分液 | ||
| C. | KCl溶液(KNO3)----降温结晶,过滤 | D. | Cl2(HCl)----饱和氯化钠溶液,洗气 |
14. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
(1)如表所列数据是该反应在不同温度下的化学平衡常数(K)
①该反应的熵变△S<0 ( 填:“<,>,=”).该反应在低温(填:高温或低温)条件下能自发进行.
②要提高CO的转化率,可以采取的措施是df(填序号).
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
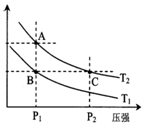
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A<C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)(1)如表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②要提高CO的转化率,可以采取的措施是df(填序号).
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A<C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
4.下列说法或实验操作正确的是( )
| A. | 决定反应速率的主要因素有浓度、压强、温度 | |
| B. | 容量瓶、量筒个滴定管上都标有使用温度,容量瓶无“0”刻度,量筒、滴定管有“0”刻度;实验时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| C. | 为实验安全,金属钠切割下来的表层物质反应放回原试剂瓶,不能再研磨氯酸钾或硝酸钾 | |
| D. | 皂化反应结束后的混合液中加入饱和食盐水,再通过分液操作分离出硬质酸钠 |
11.将NO2装入带有活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,改变某个条件,下列叙述正确的是( )
| A. | 升高温度,气体颜色加深,则此反应为吸热反应 | |
| B. | 慢慢压缩气体体积,平衡向正反应方向移动,混合气体的颜色变浅 | |
| C. | 慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 | |
| D. | 恒温恒容时,充入惰性气体,压强增大,平衡向正反应方向移动,混合气体的颜色变浅 |
9.电解质是一类在水溶液里或熔融状态下能够导电的化合物.下列物质属于电解质的是( )
| A. | Cu | B. | K2SO4 | C. | MgCl2溶液 | D. | 盐酸 |