题目内容
20.短周期元素W、Q、X、Y在元素周期表中的位置如图,其中X是两性金属元素.则( )| W | Q | ||
| X | Y |
| A. | 简单离子半径:X<Q | B. | 气态氢化物的稳定性:Y>Q | ||
| C. | X的族序数大于周期数 | D. | Y氧化物对应水化物是强酸 |
分析 X是两性金属元素,则X为Al,结合元素在短周期的位置可知,W为N,Q为O,Y为S,
A.具有相同电子排布的离子中,原子序数大的离子半径小;
B.非金属性越强,对应氢化物越稳定;
C.X位于第三周期第ⅢA族;
D.Y氧化物对应水化物为亚硫酸或硫酸.
解答 解:X是两性金属元素,则X为Al,结合元素在短周期的位置可知,W为N,Q为O,Y为S,
A.具有相同电子排布的离子中,原子序数大的离子半径小,则简单离子半径:X<Q,故A正确;
B.非金属性越强,对应氢化物越稳定,则气态氢化物的稳定性:Y<Q,故B错误;
C.X位于第三周期第ⅢA族,则X的族序数等于周期数,故C错误;
D.Y氧化物对应水化物为亚硫酸或硫酸,若为亚硫酸,属于弱酸,故D错误;
故选A.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、元素的性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
10. 紫菜与海带类似,是一种富含生物碘的海洋植物.商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取.
紫菜与海带类似,是一种富含生物碘的海洋植物.商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取.
(1)实验室中焙烧紫菜用到的仪器有DFGH(填写相应的字母).
A.烧杯 B.表面皿 C.蒸发皿 D.坩埚
E.试管 F.酒精灯 G.三脚架 H.泥三角
(2)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,其目的是将溶液中的I-转化为I2.
(3)过滤 (填一种基本操作的名称),弃去残渣,将所得的产物转入分液漏斗 (填一种玻璃仪器的名称)中,加入少量的四氯化碳 (填本题表格中一种最佳化学试剂的名称),振荡、静置,首先将紫色下层液体分离出来.
(4)将如图装置图中缺少的必要仪器补画出来以最终获得固态的单质碘(不考虑碘的进一步提纯): .
.
 紫菜与海带类似,是一种富含生物碘的海洋植物.商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取.
紫菜与海带类似,是一种富含生物碘的海洋植物.商品紫菜轻薄松脆、比海带更易被焙烧成灰(此时碘转化为碘化物无机盐),用于碘单质的提取.| 乙醇 | 四氯化碳 | 碘(晶体) | |
| 密度/g•cm-3 | 0.7893 | 1.595 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 184.35 |
A.烧杯 B.表面皿 C.蒸发皿 D.坩埚
E.试管 F.酒精灯 G.三脚架 H.泥三角
(2)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,其目的是将溶液中的I-转化为I2.
(3)过滤 (填一种基本操作的名称),弃去残渣,将所得的产物转入分液漏斗 (填一种玻璃仪器的名称)中,加入少量的四氯化碳 (填本题表格中一种最佳化学试剂的名称),振荡、静置,首先将紫色下层液体分离出来.
(4)将如图装置图中缺少的必要仪器补画出来以最终获得固态的单质碘(不考虑碘的进一步提纯):
 .
.
8.某有机物结构如图所示,有关该物质的叙述正确的是( )


| A. | 易溶于水 | |
| B. | 一氯代物有5种 | |
| C. | 最多能与氢气以物质的量之比1:4加成 | |
| D. | 碱性水解的产物之一是1-丙醇 |
15.可用浓硫酸干燥的气体是( )
| A. | SO2 | B. | H2S | C. | HBr | D. | NH3 |
5.下列各项应用涉及的化学原理完全相同的是( )
| A. | 用氯化铁或液氯处理废水 | |
| B. | 用铁槽车或铝槽车运输浓硫酸 | |
| C. | 用二氧化硫或氯气漂自织物 | |
| D. | 用亚硫酸钠或氯水处理二氧化硫尾气 |
12.下列选项中的气体能用如图装置制备,且所选试剂、干燥剂均正确的是( )
| 气体 | 所用试剂 | 干燥剂 | 装置(可加热) | |
| A | O2 | 氯酸钾和二氧化锰 | 无水氯化钙 | 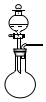 |
| B | NH3 | 浓氨水和生石灰 | 碱石灰 | |
| C | H2 | 稀硝酸和锌粒 | 浓硫酸 | |
| D | SO2 | 浓盐酸和亚硫酸钠 | 碱石灰 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法不正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 丙烷和2-甲基丙烷的一氯代物均为两种 | |
| C. | 油脂发生皂化反应能生成甘油 | |
| D. | 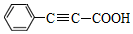 是高分子化合物 是高分子化合物 的单体 的单体 |
15.已知25℃时:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H1=-67.7kJ•mol-1
②H+(aq)+OH-(aq)=H2O(l)△H2=-57.3kJ•mol-1
③Ba2+(aq)+SO42-(aq)=BaSO4(s)△H3<0
下列说法正确的是( )
①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H1=-67.7kJ•mol-1
②H+(aq)+OH-(aq)=H2O(l)△H2=-57.3kJ•mol-1
③Ba2+(aq)+SO42-(aq)=BaSO4(s)△H3<0
下列说法正确的是( )
| A. | HF的电离方程式及热效应:HF(aq)?H+(aq)+F-(aq)△H>0 | |
| B. | 在氢氧化钠溶液与盐酸的反应中,氢氧化钠溶液量越多,中和热越大 | |
| C. | △H2=-57.3 kJ•mol-1是强酸和强碱在稀溶液中反应生成可溶盐的中和热 | |
| D. | 稀硫酸与稀氢氧化钡溶液反应的热化学方程式为H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ•mol-1 |
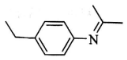 )有广泛应用.合成G的一种路径如图.1H-NMR谱显示C结构中只有一种环境的氢,且不能发生银镜反应,D的组成为C8H10.
)有广泛应用.合成G的一种路径如图.1H-NMR谱显示C结构中只有一种环境的氢,且不能发生银镜反应,D的组成为C8H10.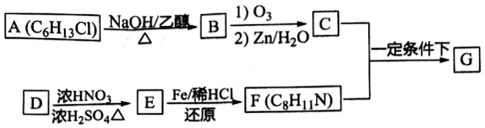
 $→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+
$→_{②Zn/H_{2}O}^{①O_{3}}$R1CHO+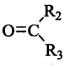
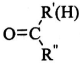 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +H2O
+H2O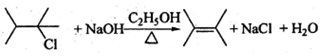 .
. .
.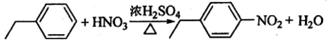 .
.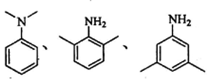 .
.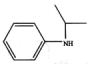 )的合成路线(流程图表示,无机试剂任选)
)的合成路线(流程图表示,无机试剂任选)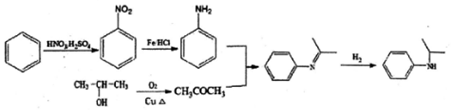 .
.