题目内容
10.下列叙述中,正确的是( )| A. | 含金属元素的离子不一定都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 最高价含氧酸一定具有强氧化性 | |
| D. | 金属阳离子被还原一定得到金属单质 |
分析 A.含金属元素的离子不一定都是阳离子,如AlO2-、MnO4-等,为阴离子;
B.氧化还原反应中,非金属也可为还原剂;
C.元素处于最高价时只具有氧化性,但是氧化性的强弱要根据具体的物质来确定;
D.如金属存在多种化合价,被还原生成较低价态的金属离子.
解答 解:A.含金属元素的离子不一定都是阳离子,如AlO2-、MnO4-等,为阴离子,故A正确.
B.S可与浓硝酸反应,反应中S为还原剂,S与氢气反应中S为氧化剂,则非金属可为氧化剂,也可为还原剂,故B错误;
C.元素处于最高价时只具有氧化性,但是氧化性的强弱要根据具体的物质来确定,如H2CO3就是碳元素的最高价含氧酸,但其没有强氧化性,故C错误;
D.金属存在多种化合价,被还原生成较低价态的金属离子,例如Fe3+被还原可生成Fe2+,故D错误;
故选:A.
点评 本题考查氧化还原反应,为考试高频考点,侧重于学生的分析能力的考查,注意从元素化合价的角度判断相关概念并认识相关物质的性质,难度不大,答题时注意能举出实例.

练习册系列答案
相关题目
20.NA是阿伏加德罗常数,下列说法一定正确的是( )
| A. | 5.6g铁与稀硝酸完全反应,转移的电子数为0.2NA | |
| B. | 标准状况下,22.4L氢气和22.4L氦气所含的质子数均为0.2NA | |
| C. | 100mL2mol•L-1 碳酸钠溶液中,CO32-数为0.2NA | |
| D. | 标准状况下,22.4LSO3所含原子数为3 NA |
15.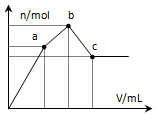 向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
 向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A. | a点的溶液呈中性 | |
| B. | 从开始到b点发生反应的总的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ | |
| C. | c点加入Ba(OH)2溶液的体积为200 mL | |
| D. | c点溶液呈碱性 |
2.下列各化合物的命名正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | |
| B. | CH3COOCH2CH2OOCCH3 乙二酸二乙酯 | |
| C. | CH3CH2CH(OH)CH3 3-丁醇 | |
| D. |  2-甲基丁烷 2-甲基丁烷 |
20.化学与人类生产、生活、社会可持续发展密切相关.下列有关说法正确的是( )
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2═2O3有单质参加,属于氧化还原反应 | |
| D. | 向水中加入明矾进行杀菌消毒 |
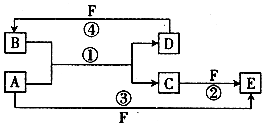 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出) ,反应④的化学方程式为(F为浓溶液)C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
,反应④的化学方程式为(F为浓溶液)C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
