题目内容
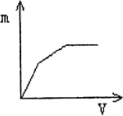
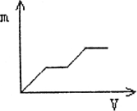
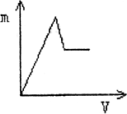
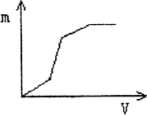
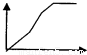
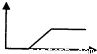
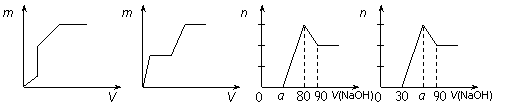
向盐酸酸化的MgSO4溶液中加入0.1mol/LBa(OH)2溶液,产生的沉淀物质的量n(纵坐标)与加入Ba(OH)2溶液的体积V(横坐标)之间的关系一定不正确的是( )
分析:盐酸酸化的MgSO4溶液存在H+、Mg2+和SO42-离子,加入Ba(OH)2溶液,首先发生Ba2++SO42-=BaSO4↓、H++OH-=H2O,然后发生Mg2++2OH-=Mg(OH)2↓,则一开始就应有沉淀生成.
解答:解:盐酸酸化的MgSO4溶液存在H+、Mg2+和SO42-离子,加入Ba(OH)2溶液,首先发生Ba2++SO42-=BaSO4↓、H++OH-=H2O,然后发生Mg2++2OH-=Mg(OH)2↓,则一开始就应有沉淀生成,由于盐酸的两不确定,而曲线的变化特点不确定,但可以肯定的是D一定错误,因开始没有沉淀生成,不符合反应实际.
故选D.
故选D.
点评:本题考查离子反应问题,题目难度中等,注意把握离子反应的先后顺序,为解答该题的关键.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目