题目内容
11.下列过程属于放热反应的是( )| A. | 浓硫酸溶于水 | B. | 碳与水蒸气的反应 | ||
| C. | 氯酸钾受热分解 | D. | 酸碱中和 |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化合反应、铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化、某些复分解(如铵盐和强碱).
解答 解:A.浓硫酸加水稀释是物理变化,故A错误;
B.碳与水蒸气的反应是吸热反应,故B错误;
C.氯酸钾受热分解是分解反应,属于吸热反应,故C错误;
D.酸碱中和是放热反应,故D正确,
故选D.
点评 本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是本题解题的关键.

练习册系列答案
相关题目
20.下列关于有机物的说法正确的是( )
| A. | 糖类、油脂、蛋白质在一定条件下均能水解 | |
| B. | 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物 | |
| C. | 分子式为C4H8C12的有机物共有(不含立体异构)8种 | |
| D. | 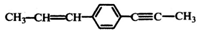 处于同一平面上的原子数最多为18个 处于同一平面上的原子数最多为18个 |
6.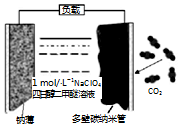 可充电“钠•二氧化碳”电池(如图),电池总反应为:4Na+3CO2$?_{充电}^{放电}$ 2Na2CO3+C,下列说法错误的是( )
可充电“钠•二氧化碳”电池(如图),电池总反应为:4Na+3CO2$?_{充电}^{放电}$ 2Na2CO3+C,下列说法错误的是( )
 可充电“钠•二氧化碳”电池(如图),电池总反应为:4Na+3CO2$?_{充电}^{放电}$ 2Na2CO3+C,下列说法错误的是( )
可充电“钠•二氧化碳”电池(如图),电池总反应为:4Na+3CO2$?_{充电}^{放电}$ 2Na2CO3+C,下列说法错误的是( )| A. | 放电时,Na+向正极移动 | |
| B. | 放电时,电子从钠薄经负载流向多壁纳米碳管 | |
| C. | 充电时,钠薄和外接电源的负极相连,发生氧化反应 | |
| D. | 充电时,阳极的电极反应为:2Na2CO3+C-4e-═4Na++3CO2↑ |
16.现有部分元素的性质、用途与原子(或分子)结构如表所示:
(1)元素Y在周期表中的位置第二周期ⅡA族,元素T的简单离子结构示意图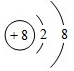 .
.
(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式 .
.
(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲+乙 $\frac{\underline{\;\;△\;\;}}{\;}$ 丙+丁,该反应为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(4)元素X与元素W以原子个数比1:2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1:1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式N2H4+2H2O2=N2↑+4H2O.
| 元素编号 | 元素性质与原子(或分子)结构 |
| W | 周期表中原子半径最小的元素 |
| X | 氢化物可与其最高价氧化物的水化物反应生成盐 |
| Y | 一种核素在考古时常用来鉴定一些文物的年代 |
| Z | M层比K层少1个电子 |
| T | 存在两种同素异形体,其中一种可吸收紫外线 |
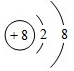 .
.(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式
 .
.(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲+乙 $\frac{\underline{\;\;△\;\;}}{\;}$ 丙+丁,该反应为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(4)元素X与元素W以原子个数比1:2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1:1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式N2H4+2H2O2=N2↑+4H2O.
1.下列说法正确的是( )
| A. | Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) | |
| B. | 向醋酸溶液中加水,醋酸的电离程度增大,$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$增大 | |
| C. | 向氨水中滴加盐酸时,离子浓度大小可能是:c(NH4+)>c(OH-)>c(Cl-)>c(H+) | |
| D. | 若NaHA溶液中的pH>7,则H2A是弱酸;若NaHA溶液中的pH<7,则H2A是强酸 |
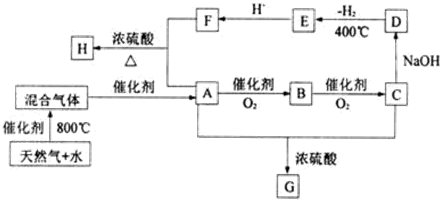
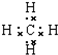 ;E的化学式是Na2C2O4.
;E的化学式是Na2C2O4.