题目内容
在25℃时,pH=1的溶液中,下列各组离子可以大量共存的是( )
| A、Na+、Ca2+、Cl-、HCO3- |
| B、Na+、Fe3+、Cl-、HCO3- |
| C、Fe2+、Fe3+、Cl-、NO3- |
| D、Fe2+、Mg2+、Cl-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:pH=1的溶液呈酸性,如离子之间不发生复分解、氧化还原反应或互促水解反应,则可大量共存,反之不能.
解答:
解:A.酸性条件下HCO3-不能大量共存,故A错误;
B.Fe3+、HCO3-发生互促水解反应,且HCO3-在酸性条件下不能大量共存,故B错误;
C.酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故C错误;
D.离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.Fe3+、HCO3-发生互促水解反应,且HCO3-在酸性条件下不能大量共存,故B错误;
C.酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故C错误;
D.离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子共存问题,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关离子的性质,注意题目酸性的特点,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H=?的化学反应,下列叙述不正确的是( )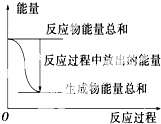

| A、反应过程中能量关系如上图表示,则该反应为放热反应 |
| B、若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
| C、化学反应的焓变与反应方程式的计量数有关 |
| D、若将该反应设计成原电池,锌为负极 |
下列有关气体体积的叙述正确的是( )
| A、一定温度和压强下,各种气态物质的体积大小,由构成气体的分子大小决定的 |
| B、不同的气体,若体积不同,则他们的分子数也不同 |
| C、一定温度和压强下,各种气态物质的体积大小,由构成气体的分子数决定的 |
| D、气体摩尔体积是指1 mol任何气体所占的体积约为22.4L |
有2份质量分数不同的NaHCO3和NaOH的混合物,将它们分别用酒精灯加热至恒重测得的数据如下:经分析得到的15.600g固体是纯净物.则下列叙述正确的是( )
| 第1份 | 第2份 | |
| 混合物质量(g) | 9.2 | 18.4 |
| 反应后固体质量(g) | 8.3 | 15.6 |
| A、本次实验至少要进行6次称重 |
| B、第1份混合物中NaOH的质量分数更大 |
| C、根据表中数据不能计算出第1份混合物中NaHCO3的质量分数 |
| D、第2份混合物中NaOH的质量分数小于0.32 |
稀释某弱酸HA溶液时,浓度增大的是( )
| A、HA |
| B、H+ |
| C、A- |
| D、OH- |
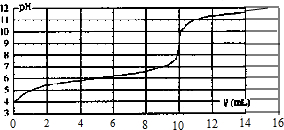 实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )
实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )| A、此一元弱酸HA的电离平衡常数Ka≈1×10-4mol?L-1 |
| B、此弱酸的起始浓度约为1×10-2mol?L-1 |
| C、此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂 |
| D、当混合液pH=7时,溶液中c(HA)>c(A-) |