题目内容
写出下列物质的电子式
(1)NaOH
(2)N2
(3)CH4
(4)H2O
(5)CO2
(6)MgCl2 .
(1)NaOH
(2)N2
(3)CH4
(4)H2O
(5)CO2
(6)MgCl2
考点:电子式
专题:化学键与晶体结构
分析:(1)NaOH是由钠离子和氢氧根离子构成的离子化合物,氢氧根离子中O与H以共价键相结合;
(2)氮气中存在3对共用电子对,氮原子最外层达到8个电子;
(3)甲烷分子中碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,据此写出甲烷的电子式;
(4)水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键;
(5)二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子;
(6)氯化镁为离子化合物,必须标出阴阳离子的电子式.
(2)氮气中存在3对共用电子对,氮原子最外层达到8个电子;
(3)甲烷分子中碳原子最外层有4个电子,能形成4个共价键达到稳定结构,每个氢原子能形成一个共价键达到稳定结构,据此写出甲烷的电子式;
(4)水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键;
(5)二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子;
(6)氯化镁为离子化合物,必须标出阴阳离子的电子式.
解答:
解:(1)NaOH是由钠离子和氢氧根离子构成的离子化合物,氢氧根离子中O与H以共价键相结合,其电子式为 ,
,
故答案为: ;
;
(2)氮气中存在氮氮三键,氮原子最外层为达到8电子稳定结构,氮气的电子式为 ,
,
故答案为: ;
;
(3)因碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为: ,
,
故答案为: ;
;
(4)水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为: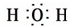 ,
,
故答案为: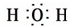 ;
;
(5)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为: ,
,
故答案为: ;
;
(6)氯化镁为离子化合物,化学式中存在阴阳离子,其电子式中需要标出阴阳离子所带电荷,氯化镁的电子式为: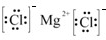 ,
,
故答案为: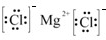 .
.
 ,
,故答案为:
 ;
;(2)氮气中存在氮氮三键,氮原子最外层为达到8电子稳定结构,氮气的电子式为
 ,
,故答案为:
 ;
;(3)因碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,所以电子式为:
 ,
,故答案为:
 ;
;(4)水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为:
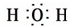 ,
,故答案为:
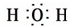 ;
;(5)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为:
 ,
,故答案为:
 ;
;(6)氯化镁为离子化合物,化学式中存在阴阳离子,其电子式中需要标出阴阳离子所带电荷,氯化镁的电子式为:
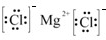 ,
,故答案为:
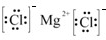 .
.
点评:本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及书写原则,明确离子化合物与共价化合物的电子式表示方法及区别.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
对三联苯( )是一种有机合成的中间体.下列关于对三联苯的说法中正确的是( )
)是一种有机合成的中间体.下列关于对三联苯的说法中正确的是( )
 )是一种有机合成的中间体.下列关于对三联苯的说法中正确的是( )
)是一种有机合成的中间体.下列关于对三联苯的说法中正确的是( )| A、对三联苯属于苯的同系物 |
| B、对三联苯分子中至少有16个原子共平面 |
| C、对三联苯的一氯取代物有6种 |
| D、0.2mol对三联苯在足量的氧气中完全燃烧消耗5.1mol O2 |
塑化剂是一种对人体有害的物质,曾在某些白酒中被检测出来.增塑剂DCHP可由邻苯二甲酸酐与环己醇反应制得:

下列说法正确的是( )

下列说法正确的是( )
| A、邻苯二甲酸酐的二氯代物有3种 |
| B、环己醇可以使溴水、酸性高锰钾溶液褪色 |
| C、1mol DCHP碱性条件完全水解时消耗4mol NaOH |
| D、DCHP属于酯类化合物,能发生加成、取代反应 |