题目内容
17.把除去氧化膜的镁条投入到盛有稀HCl的试管中,发现氢气发生的速率变化情况如图1所示.
(1)其中t1~t2速率变化的主要原因是镁条与盐酸反应放热,温度升高使反应速率加快.
(2)t2~t3速率变化的主要原因是盐酸浓度减小,反应速率减慢.
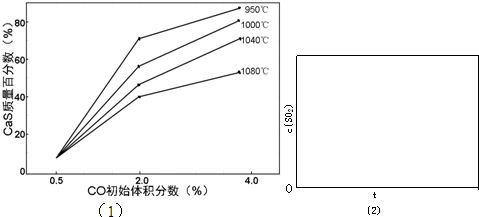
(3)在图2中画出生成H2的体积随时间变化的示意图.
分析 金属镁与盐酸反应生成氯化镁和氢气,反应放热,影响速率的因素有浓度和温度,以此解答该题.
解答 解:(1)金属镁与酸的反应为放热反应,反应开始时,温度不断升高,则反应速率逐渐增大,故答案为:镁条与盐酸反应放热,温度升高使反应速率加快;
(2)但随着反应的极性,反应物的浓度逐渐降低,此时浓度的影响大于温度的影响,反应速率反而减小,故答案为:盐酸浓度减小,反应速率减慢;
(3)反应速率先增大后减小,生成氢气的体积不断增大,但曲线的斜率先增大后减小,图象可为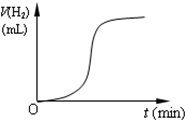 ,
,
故答案为: .
.
点评 本题考查影响化学反应速率的因素,为高频考点,把握温度、浓度对反应速率的影响及图象分析为解答的关键,注重分析与知识应用能力的考查,题目难度不大.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
11.某温度下纯水的c(H+)=1.0×10-6mol/L,在此温度下,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合(溶液体积变化忽略不计).欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为( )
| A. | 11:1 | B. | 9:2 | C. | 1:11 | D. | 2:9 |
5.下列说法正确的是( )
| A. | 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小 | |
| B. | 乙烯与溴发生加成反应的产物为溴乙烷 | |
| C. | n=7,主链上有5个碳原子的烷烃共有五种 | |
| D. | 1mol苯恰好与3mol氢气完全加成,说明一个苯分子中有三个碳碳双键 |
2.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,22.4LSO3中含有O数目为3.0NA | |
| B. | 常温常压下,12.2gNaHSO4中含有离子总数为0.3NA | |
| C. | 在1L 0.1mol•L-1碳酸钠溶液中,阴离子总数大于0.1NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
6.设NA为阿伏加德罗常数的值,下列有关叙述中正确的是( )
| A. | CH4与P4的分子结构都是正四面体形,因此在NA个CH4分子或P4分子中都含有4NA个共价键 | |
| B. | 在含NA个硅原子的二氧化硅晶体中含有4NA个Si-O键 | |
| C. | 5.6 g Fe与含0.2 mol HNO3的溶液充分反应,至少失去0.2NA个电子 | |
| D. | NA个Fe3+完全水解可以得到NA个氢氧化铁胶体粒子 |