题目内容
3.液态或固态氢在超高压下解离成氢原子,氢原子像金属原子一样堆积在一起变成导电体,故称为“金属氢”.下列关于“金属氢”的说法不正确的是( )| A. | 不能与氧气反应 | B. | 储存巨大能量 | ||
| C. | 是氢的一种同素异形体 | D. | 内部存在自由移动的电子 |
分析 A、金属氢极易失电子,与氧气发生氧化还原反应;
B、液态或固态氢在超高压下解离成氢原子,此时吸收大量的能量;
C、金属氢是氢的一种同素异形体;
D、氢原子像金属原子一样堆积在一起变成导电体.
解答 解:A、金属氢极易失电子,与氧气发生氧化还原反应,所以能与氧气反应,故A错误;
B、液态或固态氢在超高压下解离成氢原子,此时吸收大量的能量,所以金属氢中储存巨大能量,故B正确;
C、金属氢是氢的一种同素异形体,故C正确;
D、氢原子像金属原子一样堆积在一起变成导电体,说明内部存在自由移动的电子,故D正确;
故选A.
点评 本题考查氢的同素异形体及同素异形体的性质,学生在解题中要始终抓住题目信息,这是解题的关键,比较容易.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
13.真空碳热还原氯化法可实现由铝矿制备金属铝,其相关的热化学方程
①Al2O3(S)+3C(S)═2Al(S)+3CO(g)△H1═+1344.1KJ•mol-1
②2AlCl3(g)═2Al(S)+3Cl2(g)△H2═+1169.2KJ•mol-1
③Al2O3(g)+3C(S)+3Cl2(g)═2AlCl3(g)+3CO(g)△H3═+QKJ•mol-1
下列有关说法正确的是( )
①Al2O3(S)+3C(S)═2Al(S)+3CO(g)△H1═+1344.1KJ•mol-1
②2AlCl3(g)═2Al(S)+3Cl2(g)△H2═+1169.2KJ•mol-1
③Al2O3(g)+3C(S)+3Cl2(g)═2AlCl3(g)+3CO(g)△H3═+QKJ•mol-1
下列有关说法正确的是( )
| A. | 反应①中化学能转化为热能 | |
| B. | 反应②中若生成液态铝则反应热应大于△H2 | |
| C. | 反应③中1molAlCl3(g)生成时,需要吸收174.9kJ的热量 | |
| D. | 该生产工艺中能循环利用的物质只有A1C13 |
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 28g乙烯和丙烯的混合物中所含碳碳双键的数目为NA | |
| B. | 1L0.5mol•L-1Na2CO3溶液中阴离子的总数为0.5NA | |
| C. | 标准状况下,11.2L H2和D2的混合气体中所含的质子数为NA | |
| D. | 向大量水中通入1mol氯气,反应中转移的电子数为NA |
11.用下列实验装置进行相应实验,能达到实验目的是( )
| A. | 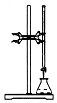 用标准氢氧化钠溶液滴定未知浓度的盐酸 | |
| B. | 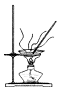 加热FeCl3溶液获取FeCl3固体 | |
| C. | 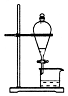 用酒精萃取碘水中的碘 | |
| D. | 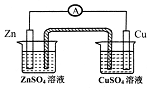 通过原电池原理证明金属性Zn>Cu |
8.化学与生活有密切联系,下列说法正确的是( )
| A. | 酸雨易导致土壤胶粒吸附H+使土壤酸化,影响铵态氮肥和钾肥的有效利用 | |
| B. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| C. | 高纯度的单晶硅用于制造登月车的光电池和光导纤维 | |
| D. | 铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝 |
15.下列各组中两种微粒所含电子数不相等的是( )
| A. | S2-和Al3+ | B. | CO和N2 | C. | H3O+和OH- | D. | NH3和NH4+ |
12. 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法不正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法不正确的是( )
 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法不正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法不正确的是( )| A. | 每“呼出”22.4LCO2,转移电子数为$\frac{4}{3}$mol | |
| B. | “吸入”CO2时的正极反应:4Na++3CO2+4e-=2Na2CO3+C | |
| C. | “呼出”CO2时钠箔电极反应式是Na++e-=Na | |
| D. | 放电时电池总反应是4Na+3CO2=2Na2CO3+C |
5.碘在科研与生活中有重要作用,某兴趣小组用0.50mol•L-1KI、0.2%淀粉溶液、0,.20mol•L-1K2S2O8、0.10mol•L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
已知:
S2O82-+2I-═2SO42-+I2(慢)
I2+2S2O32-═2I-+S4O62- (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O82-):n(S2O32-)$>\frac{1}{2}$.
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如表:
表中Vx=2.0 ml,理由是保证反应物K2S2O8浓度改变,而其他的条件不变,才能达到实验目的.
(3)已知:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你的猜想还可能是生成的锰离子有催化作用的影响.
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是C.
A.硫酸钾 B.氯化锰 C.硫酸锰 D.水.
已知:
S2O82-+2I-═2SO42-+I2(慢)
I2+2S2O32-═2I-+S4O62- (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O82-):n(S2O32-)$>\frac{1}{2}$.
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如表:
| 实验 序号 | 体积V/ml | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
(3)已知:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你的猜想还可能是生成的锰离子有催化作用的影响.
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是C.
A.硫酸钾 B.氯化锰 C.硫酸锰 D.水.
 配合物[Cu(CH3C≡N)4]BF4是双烯合成反应的催化剂,它被浓硝酸分解的化学方程式为:[Cu(CH3C≡N)4]BF4$\stackrel{HNO_{3}}{→}$Cu2++H3BO3+CO2↑+HF…(未配平).
配合物[Cu(CH3C≡N)4]BF4是双烯合成反应的催化剂,它被浓硝酸分解的化学方程式为:[Cu(CH3C≡N)4]BF4$\stackrel{HNO_{3}}{→}$Cu2++H3BO3+CO2↑+HF…(未配平).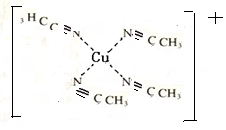 (不考虑空间构型).
(不考虑空间构型).