题目内容
2.实验室用密度为1.25g/mL,质量分数为36.5%的浓盐酸配置240mL 0.1mol/L的盐酸.浓盐酸的物质量浓度为多少?配置稀盐酸应取用的浓盐酸的体积为多少?分析 根据c=$\frac{1000ρw}{M}$计算浓盐酸的物质量浓度;根据c(浓)×V(浓)=c(稀)×V(稀)计算取用的浓盐酸的体积.
解答 解:c=$\frac{1000ρw}{M}$=$\frac{1000×36.5%×1.25}{36.5}$mol/L=12.5 mol/L;
溶液稀释前后溶质的物质的量不变,则有c(浓)×V(浓)=c(稀)×V(稀),又配置240mL 0.1mol/L的盐酸,应选择250mL的容量瓶,计算按照250mL计算,所以 V浓=$\frac{{{C_稀}•{V_稀}}}{C_浓}$=$\frac{0.25×0.1}{12.5}$L=0.002L=2ml;
答:此浓盐酸的物质的量浓度是12.5mol/L;则需要取用的浓盐酸的体积2mL.
点评 本题考查物质的量浓度的计算,题目难度不大,注意质量分数与物质的量浓度之间的换算关系.

练习册系列答案
相关题目
13.将10℃的0.2mol N2O4置于2L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g)?2NO2 (g).下列结论能说明上述反应在该条件下已经达到平衡状态的是( )
①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化.
①烧瓶内气体的平均相对分子质量不再变化
②NO2的物质的量浓度不再改变
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤烧瓶内气体的颜色不再加深
⑥N2O4的消耗速率与NO2的生成速率之比为1:2
⑦NO2生成速率与NO2消耗速率相等
⑧烧瓶内气体的密度不再变化.
| A. | ①②③⑤⑦ | B. | ①②③⑤⑥⑦ | C. | ①②③④ | D. | ②③⑦⑧ |
10.不能用有关胶体的观点解释的现象是( )
| A. | 在江河入海处易形成三角洲 | |
| B. | AgNO3溶液中滴入同浓度NaCl溶液,生成白色沉淀 | |
| C. | 卤水点豆腐 | |
| D. | 同一钢笔同时使用不同牌号的墨水易发生堵塞 |
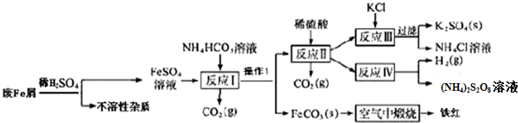
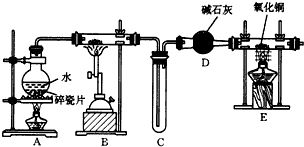
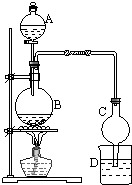 (1)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中盛有浓硫酸,B中盛有乙醇、乙酸,D中盛有饱和碳酸钠溶液.
(1)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中盛有浓硫酸,B中盛有乙醇、乙酸,D中盛有饱和碳酸钠溶液.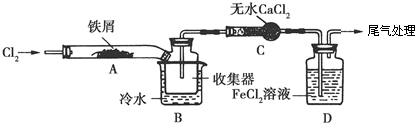
 .FeCl3是共价化合物(填“离子”或“共价”).
.FeCl3是共价化合物(填“离子”或“共价”).