题目内容
2.下列表示物质结构的化学用语或模型图正确的是( )| A. | 次氯酸电子式 | B. | 核内有8个中子的碳原子${\;}_{6}^{8}$C | ||
| C. | CO2的比例模型 | D. | 纯碱的化学式Na2CO3 |
分析 A.次氯酸中各个原子的最外层电子数均达到了稳定结构,其中的共价键有氢氧键和氯氧键;
B.质量数=质子数+中子数,该碳原子的质量数为14,元素符号的左上角表示质量数、左下角表示质子数;
C.比例模型表示原子的相对大小及原子连接顺序、空间结构;
D.纯碱的化学式Na2CO3.
解答 解:A.次氯酸中的共价键有氢氧键和氯氧键,氧原子应该放在中间位置,次氯酸的电子式为: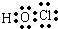 ,故A错误;
,故A错误;
B.碳原子的核电荷数为6,核内有8个中子的碳原子的质量数为14,该原子正确的表示方法为:614C,故B错误;
C.二氧化碳的分子式为CO2,由模型可知小球为碳原子,2个大球为氧原子,氧原子半径大,实际碳原子半径大于氧原子半径,故C错误;
D.纯碱是Na2CO3的俗名,故D正确.
故选D.
点评 本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、比例模型、元素符号等化学用语的概念及正确的表示方法,试题培养了学生规范答题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列说法不正确的是( )
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) | |
| B. | 将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸需加的水量多 | |
| C. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) | |
| D. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) |
8.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 用漂白粉可以净化饮用水 | |
| B. | 铜的金属性比铁弱,所以可用铜罐代替铁罐贮藏浓硝酸 | |
| C. | 合成纤维和光导纤维都是人工合成的有机高分子化合物 | |
| D. | 工业上可用石灰乳对煤燃烧形成的烟气进行脱硫,最终能制得石膏 |
10.在200mLMgCl2,AlCl3的混合溶液中,浓度为:MgCl2 2mol/L,AlCl3 3mol/L.现欲使其中的Mg2+转化为Mg(OH)2沉淀而从溶液中分离出来,至少需要0.8mol/LNaOH溶液的体积是( )
| A. | 0.533L | B. | 0.267L | C. | 4.0L | D. | 2.0L |
11.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 80gCuO和Cu2S的混合物含有的Cu原子数一定是NA | |
| B. | 标准状况下,5.6L O2作为氧化剂时转移的电子数一定为NA | |
| C. | 常温常压下,14g C2H4和C3H6混合气体中含有的原子数为3NA | |
| D. | 25℃,1LpH=13的NaOH溶液中含有OH-的数目为 0.1NA |
12.下列说法正确的是( )
| A. | 酒精、硫酸钡和水分别属于电解质、强电解质和弱电解质 | |
| B. | Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 | |
| C. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| D. | 天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源 |
