题目内容
(16分)(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性,原因是(用离子方程式表示):______ ______。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
(16分)、(1)酸,<,Cu2++ H2O 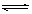 Cu(OH)2+ 2H+,抑制
Cu(OH)2+ 2H+,抑制
(2)酸,Al3++3H2O 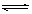 Al(OH)3+3H+, Al2O3
Al(OH)3+3H+, Al2O3
(3)NaOH。
解析试题分析:(1)硝酸铜是强酸弱碱盐,Cu2+水解显酸性,水解方程式是Cu2++ H2O 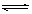 Cu(OH)2+ 2H+,所以pH<7;硝酸银也是强酸弱碱盐,水解显酸性,所以实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度的目的是抑制Ag+水解。
Cu(OH)2+ 2H+,所以pH<7;硝酸银也是强酸弱碱盐,水解显酸性,所以实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度的目的是抑制Ag+水解。
(2)氯化铝是强酸弱碱盐,Al3+水解显酸性,水解方程式是Al3++3H2O 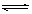 Al(OH)3+3H+,所以氯化铝溶液显酸性;由于水解是吸热的,所以加热促进水解,同时生成的氯化氢易挥发,进一步促进水解,所以最终得到的是氢氧化铝固体,灼烧得到氧化铝。
Al(OH)3+3H+,所以氯化铝溶液显酸性;由于水解是吸热的,所以加热促进水解,同时生成的氯化氢易挥发,进一步促进水解,所以最终得到的是氢氧化铝固体,灼烧得到氧化铝。
(3)硫化钠是强碱弱酸盐,S2-水解溶液显碱性,所以为了防止发生水解,可以加入少量的氢氧化钠以抑制水解。
考点:考查盐类水解应用、水解方程式的书写等。
点评:在溶液中,强碱弱酸盐,强酸弱酸盐或弱酸弱碱盐电离出来的离子与水电离出来的H+与OH-生成弱电解质的过程叫做盐类水解,水解平衡也是动态平衡,适用于勒夏特列原理。

 备战中考寒假系列答案
备战中考寒假系列答案
