题目内容
17.常温下,浓度均为0.1mlo•L-1的HX、HY溶液各20mL,分别用0.1mol•L-1的Na0H溶液滴定.溶液的pH与所用Na0H的体积V关系如图所示,下列推断不正确的是( )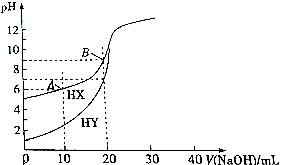
| A. | 相同条件下,HX和HY中和碱的能力相同 | |
| B. | 常温下,HX的电离平衡常数K=1×10-9mol•L-1 | |
| C. | 点存在:c(X-)-c(HX)>c(H+)-c(0H-) | |
| D. | 向B点溶液通人HCl气体至中性:c(HX)+c(Cl-)+2c(X-)=0.2mol•L-1A |
分析 A.物质的量相同的一元酸中和碱的能力相同;
B.根据氢氧化钠滴到10mL,c(HX)≈c(X-),Ka(HX)≈c(H+);
C.当溶液中c(Na+)>c(HX)时,存在c(X-)-c(HX)>c(H+)-c(0H-);
D.溶液中c(X-)+c(HX)=0.1mol/L,c(Na+)=0.1mol/L,结合电荷守恒分析.
解答 解:A.浓度均为0.1mlo•L-1的HX、HY溶液各20mL,两种酸的物质的量相同,所以中和碱的能力相同,故A正确;
B.当氢氧化钠滴到10mL,溶液中c(HX)≈c(X-),Ka(HX)≈c(H+)=1×10-6mol•L-1,故B错误;
C.当溶液中c(Na+)>c(HX)时,溶液中电荷守恒为c(X-)+c(0H-)=c(H+)+c(Na+),所以c(X-)-c(Na+)=c(H+)-c(0H-),则存在c(X-)-c(HX)>c(H+)-c(0H-),故C正确;
D.溶液中c(X-)+c(HX)=0.1mol/L,c(Na+)=0.1mol/L,溶液中电荷守恒为:c(X-)+c(Cl-)+c(0H-)=c(H+)+c(Na+),所以c(HX)+c(Cl-)+2c(X-)=0.2mol•L-1,故D正确.
故选B.
点评 本题考查了溶液酸碱性与溶液pH的计算、酸碱混合的定性判断、溶液中离子浓度大小比较,题目难度中等,注意掌握酸碱混合的定性判断及有关溶液pH的计算方法,正确分析、理解图象信息为解答本题的关键.

练习册系列答案
相关题目
7.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获2002年诺贝尔化学奖.下面有关叙述正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同素异形体 | ||
| C. | 15N 与14N 互为同位素 | D. | 232Th转化成233U是化学变化 |
8.为了防止FeCl2溶液变质,可向溶液中加入( )
| A. | 铁粉 | B. | 铜粉 | C. | HCl溶液 | D. | 硝酸溶液 |
5.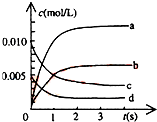 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量的浓度是0.0035mol/L;
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
9.医学上,科学家们设计以Pt和Zn为电极材料的电池,植入人体内作为心脏病患者的心脏起搏器的能源,它依靠人体内体液中存在的一定浓度的溶解的O2、H+、Zn2+进行工作.下列叙述正确的是( )
| A. | Pt为负极,Zn为正极 | |
| B. | Zn为负极,Pt为正极 | |
| C. | 负极反应式为Zn-2e-═Zn2+,正极反应式为2H++2e-═H2↑ | |
| D. | 负极反应式为Zn-2e-═Zn2+,正极反应式为O2+2H2O+4e-═4OH- |
9.下列清洁剂能与常用的肥皂最为接近的是( )
| A. | CH3-(CH2)11C6H4-SO3Na | B. | CH3-(CH2)13-COOK | ||
| C. | CH3-(CH2)11-SO3Na | D. | CH3(CH2)nCH3(5≤n≤12) |
10.用苦卤(含Na+、K+、Mg2+、Cl-、Br-等)可提取溴,其生产流程如下:

则下列说法中,错误的是( )

则下列说法中,错误的是( )
| A. | 反应③的离子方程式为5Br-+BrO3-+6H+═3Br2+3H2O | |
| B. | ②③的目的是富集溴,提高Br2的浓度 | |
| C. | 蒸馏塔温度控制在90℃左右的原因是防止温度过高将水蒸馏出来 | |
| D. | 从海水中提取任何化学物质都需要经过化学变化 |