题目内容
下列说法不正确的是( )
| A、pH=3的醋酸与pH=11的NaOH溶液等体积混合后,溶液的pH一定小于7 |
| B、不能使酚酞试液变红的溶液一定呈酸性 |
| C、pH=5的溶液和pH=3的溶液相比,前者c(OH-)是后者的100倍 |
| D、在1mol?L-1的氨水中,改变外界条件使c(NH4+)增大,溶液的pH不一定增大 |
考点:pH的简单计算,探究溶液的酸碱性
专题:
分析:A.pH=3的醋酸与pH=11的NaOH溶液等体积混合后,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性;
B.根据酚酞的变色范围判断,不能使酚酞试液变红的溶液可能是盐的中性溶液;
C.根据Kw=c(H+)×c(OH-)计算解答;
D.根据改变外界条件对NH3.H2O?NH4++OH-平衡的影响解答.
B.根据酚酞的变色范围判断,不能使酚酞试液变红的溶液可能是盐的中性溶液;
C.根据Kw=c(H+)×c(OH-)计算解答;
D.根据改变外界条件对NH3.H2O?NH4++OH-平衡的影响解答.
解答:
解:A.pH=3的醋酸与pH=11的NaOH溶液等体积混合后,得到醋酸和醋酸钠的混合溶液,以醋酸的电离为主,溶液呈酸性,故A正确;
B.酚酞的变色范围是8-10,所以能使酚酞试液变红的溶液呈碱性,不能使酚酞试液变红的溶液,可能是盐的中性溶液或酸性溶液,如氯化钠盐溶液不能使酚酞试液变红,故B错误;
C.25℃时,水的离子积Kw=1×10-14,根据Kw=c(H+)×c(OH-),PH=5的溶液,c(H+)=10-5mol/L,c(OH-)=10-9mol/L,PH=3的溶液,c(H+)=10-3mol/L,c(OH-)=10-11mol/L所以25℃时,PH=5的溶液与PH=3的溶液相比,前者C(OH-)是后者的100倍.故C正确;
D.在1 mol/L的氨水中,改变外界条件使c(NH4+)增大,如加入氯化铵固体,铵根离子的浓度增大,则稀氨水中NH3.H2O?NH4++OH-存在电离平衡逆向移动,氢氧根离子的浓度减小,由水的离子积可知,氢离子的浓度增大,溶液的pH减小,故D正确;
故选B.
B.酚酞的变色范围是8-10,所以能使酚酞试液变红的溶液呈碱性,不能使酚酞试液变红的溶液,可能是盐的中性溶液或酸性溶液,如氯化钠盐溶液不能使酚酞试液变红,故B错误;
C.25℃时,水的离子积Kw=1×10-14,根据Kw=c(H+)×c(OH-),PH=5的溶液,c(H+)=10-5mol/L,c(OH-)=10-9mol/L,PH=3的溶液,c(H+)=10-3mol/L,c(OH-)=10-11mol/L所以25℃时,PH=5的溶液与PH=3的溶液相比,前者C(OH-)是后者的100倍.故C正确;
D.在1 mol/L的氨水中,改变外界条件使c(NH4+)增大,如加入氯化铵固体,铵根离子的浓度增大,则稀氨水中NH3.H2O?NH4++OH-存在电离平衡逆向移动,氢氧根离子的浓度减小,由水的离子积可知,氢离子的浓度增大,溶液的pH减小,故D正确;
故选B.
点评:本题考查了溶液的PH、酸碱指示剂的变色范围、水的离子积Kw、弱电解质的电离平衡等知识,明确Kw=c(H+)×c(OH-)以及电离平衡的影响因素是解本题关键,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 科学家研制出多种新型杀虫剂,以代替DDT,化合物A是其中一种如图.下列关于这种化合物的说法正确的是( )
科学家研制出多种新型杀虫剂,以代替DDT,化合物A是其中一种如图.下列关于这种化合物的说法正确的是( )| A、化合物A的化学式为C15H20O3 |
| B、化合物A是芳香族化合物 |
| C、化合物A可以发生加成反应、酯化反应和银镜反应 |
| D、化合物A有两种官能团 |
下列关于氯气说法不正确的是( )
| A、在氯气与水反应中,氯气作氧化剂 |
| B、氯气制漂白粉时发生的是氧化还原反应 |
| C、可以用浓硫酸除去氯气中的水蒸气 |
| D、氢气在氯气中燃烧生成白色烟雾 |
现有等物质的量浓度的下列溶液:①醋酸,②醋酸钠,③碳酸,④碳酸钠,⑤碳酸氢钠,按溶液的pH由小到大的排列顺序正确的是( )
| A、③①②④⑤ |
| B、③①⑤②④ |
| C、①③②⑤④ |
| D、①③②④⑤ |
下列各组离子一定能大量共存的是( )
| A、CO32-、OH-,Na+,H+ |
| B、Al3+,Na+,S2-,Cl- |
| C、Cl-,H+,SO42-,Cu2+ |
| D、Ba2+,HCO3-,K+,SO42- |
下列属于弱电解质的是( )
| A、BaSO4 |
| B、CH3COOH |
| C、Na2O |
| D、Cl2 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1mol OH-所含的质子数为1NA |
| B、23gNa变为Na+时失去的电子数为NA |
| C、将1 mol BaCl2 溶于水所形成的溶液中含NA个氯离子 |
| D、常温常压下,22.4 L O2和O3的混合气体所含分子数为NA |
下列有关化学用语表示正确的是( )
A、钾原子结构示意图: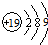 |
B、水的电子式: |
C、CO2的比例模型: |
D、间羟基苯甲酸的结构简式: |
 可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.
可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.