题目内容
2.亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:[实验Ⅰ]NaClO2晶体按如图装置进行制取.

已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.
(1)装置C起的是防止D瓶溶液倒吸到B瓶中的作用.
(2)已知装置B中的产物有ClO2气体,装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:
①减压在55℃蒸发结晶;
②趁热过滤;
③用38℃~60℃热水洗涤;
④低于60℃干燥;得到成品..
(4)反应结束后,打开K1,装置A起的作用是吸收装置B中多余的ClO2和SO2,防止污染空气;如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3.
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+4I-+4H+=2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液.取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-),则所称取的样品中NaClO2的物质的量为c•V•10-3.
分析 (1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中;
(2)装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平书写方程式;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、低温干燥的方法,注意温度控制;
(4)反应结束时,由于ClO2和SO2有毒,所以要打开K1,用氢氧化钠溶液吸收,高于60℃时NaClO2分解成NaClO3和NaCl;
(5)根据化学反应可得关系式:NaClO2~2I2~4S2O32-,令样品中NaClO2的物质的量x,根据关系式计算.
解答 解:(1)装置D中发生气体反应,装置内压强降低,装置C的作用是安全瓶,防止D瓶溶液倒吸到B瓶中,
故答案为:防止D瓶溶液倒吸到B瓶中;
(2)装置D反应后的溶液获得NaClO2晶体,装置D中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2,
故答案为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,为防止析出晶体NaClO2•3H2O,应趁热过滤,由题目信息可知,应控制温度38℃~60℃进行洗涤,低于60℃干燥,
故答案为:趁热过滤;60;
(4)反应结束时,由于ClO2和SO2有毒,所以要打开K1,用氢氧化钠溶液吸收,由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3,
故答案为:吸收装置B中多余的ClO2和SO2,防止污染空气;NaClO3;
(5)令样品中NaClO2的物质的量x,
NaClO2~2I2~4S2O32-,
1mol 4mol
0.25x c mol•L-1×V×10-3L
则:x=c•V•10-3mol
故答案为:c•V•10-3mol.
点评 本题考查制备方案的设计与评价,题目难度中等,涉及亚氯酸钠制备实验的基本操作、亚氯酸钠的性质及中和滴定等知识,理解实验原理是解题的关键,试题侧重考查学生的分析理解能力及灵活应用能力.

 名校课堂系列答案
名校课堂系列答案| A. | 原子半径呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 元素的金属性和非金属性呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
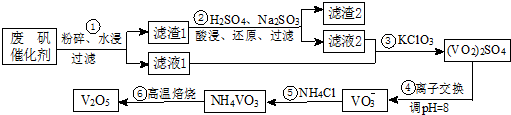
部分含钒物质在水中的溶解性见表.回答下列问题:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(2)滤渣1中含矾的物质被Na2SO3还原的离子方程式为V2O5+SO32-+4H+═2VO2++SO42-+2H2O;
请配平滤液2中VOSO4被KClO3氧化的化学方程式:6VOSO4+KClO3+3H2O═3(VO2)2SO4
+KCl+3H2SO4.
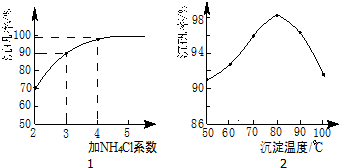
(3)步骤⑤沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中
V2O5的质量比)和温度.根据图判断沉矾最佳控制氯化铵系数和温度分别为4、80℃;从平
衡移动角度解释沉矾过程中控制n(NH4+):n(VO3-)>1:1,原因是增大铵根离子浓度,可以提高VO3-转化率,以保证VO3-沉淀完全.
(4)步骤⑥反应的化学方程式为2NH4VO3$\frac{\underline{\;\;△\;\;}}{\;}$V2O5+2NH3↑+H2O.
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+$?_{充电}^{放电}$VO2++H2O+V3+,电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+;
若用放电的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用效率为$\frac{965}{384}$m×100%(写出表达式,不必计算出结果.已知:电量Q=It,t为时间秒;电解时Q=znF,$电流利用效率=\frac{负载利用电量}{电池输出电量}×100%$
z为每摩尔物质得失电子数、法拉第常数F=96500C/mol,).
| A. | 4甲基4,5二乙基己烷 | B. | 2,3-二甲基-2,4-戊二烯 | ||
| C. | CH3CH(OH)CH2CH3:丁醇 | D. | 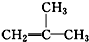 :2-甲基-1-丙烯 :2-甲基-1-丙烯 |
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素和最活泼的非金属元素分别是K、F(用元素符号作答).
(3)在这些元素的最高价氧化物对应水化物中,有一种呈两性的用来治疗胃酸过多反应的化学方程式:Al(OH)3+3HCl=AlCl3+3H2O.
(4)在这些元素中,某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,写出该方程式NH3+HNO3=NH4NO3或 H2S+3H2SO4(浓)=4SO2+4H2O.
(5)在⑤与④中,设计简单的实验(只要写出实验方案即可),证明其金属性的强弱,方案分别取大小和形状相同的Mg和Al与浓度相同的盐酸反应,观察产生气泡的速率,比较快的是Mg,故Mg金属性强;
(6)如何元素⑦与⑧的非金属性强弱,写出可以验证该结论的一个离子反应方程式S2-+Cl2=S↓+2Cl-.

 .
. .
.