题目内容
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色;Y是有刺激性气味的气体;Z常温下为无色液体.有关的转化关系如图所示(反应条件均已略去).

请回答下列问题:
(1)C的化学式为 ,“白烟”属于 晶体(填“原子”、“离子”或“分子”).
(2)反应③的离子方程式为 .
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为 .
(4)金属铜能溶于G的浓溶液中,铜有3.2g溶解时,反应中转移 mol电子.

请回答下列问题:
(1)C的化学式为
(2)反应③的离子方程式为
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)金属铜能溶于G的浓溶液中,铜有3.2g溶解时,反应中转移
考点:无机物的推断
专题:推断题
分析:X与Y产生“白烟”现象,是挥发性酸和氨气相遇后的产物,单质D与单质A反应生成X、单质D与单质B反应生成Y,由此可推知D是H2,红棕色气体F为NO2,由转化关系,结合元素守恒可推知C为O2,Z常温下为无色液体,故Z为H2O,A为Cl2,Y为NH3,X为HCl,E为NO,C为O2,G为HNO3,据此解答.
解答:
解:X与F产生“白烟”现象,是挥发性酸和氨气相遇后的产物,单质D与单质A反应生成X、单质D与单质B反应生成Y,由此可推知D是H2,红棕色气体F为NO2,由转化关系,结合元素守恒可推知C为O2,故Z为H2O,A为Cl2,Y为NH3,X为HCl,E为NO,C为O2,G为HNO3,
(1)由上述分析可知,C的化学式为O2,白烟是氯化氢和氨气形成的氯化铵固体小颗粒,为离子化合物形成离子晶体;
故答案为:O2;离子;
(2)反应③为NO2与H2O的反应,反应的离子方程式为:3NO2+H2O=2H++2NO3-+NO,
故答案为:3NO2+H2O=2H++2NO3-+NO;
(3)E为NO,为污染性气体,在一定条件下可与NH3反应生成N2和H2O,反应的化学方程式为4NH3+6NO=5N2+6H2O,
故答案为:4NH3+6NO=5N2+6H2O.
(4)金属铜能溶于G为HNO3的浓溶液中反应生成二氧化氮,硝酸铜和水,反应过程中电子转移依据反应的铜计算,有3.2g溶解时电子转移=
×2=0.1mol;
故答案为:0.1.
(1)由上述分析可知,C的化学式为O2,白烟是氯化氢和氨气形成的氯化铵固体小颗粒,为离子化合物形成离子晶体;
故答案为:O2;离子;
(2)反应③为NO2与H2O的反应,反应的离子方程式为:3NO2+H2O=2H++2NO3-+NO,
故答案为:3NO2+H2O=2H++2NO3-+NO;
(3)E为NO,为污染性气体,在一定条件下可与NH3反应生成N2和H2O,反应的化学方程式为4NH3+6NO=5N2+6H2O,
故答案为:4NH3+6NO=5N2+6H2O.
(4)金属铜能溶于G为HNO3的浓溶液中反应生成二氧化氮,硝酸铜和水,反应过程中电子转移依据反应的铜计算,有3.2g溶解时电子转移=
| 3.2g |
| 64g/mol |
故答案为:0.1.
点评:本题考查物质的推断,题目难度中等,本题注意从物质反应的典型现象作为该题的突破口,注意对元素化合物性质的掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在海水中含有多种元素,开发利用这些资源是科学研究的重要课题.如图为海水利用的部分过程.下列有关说法正确的是( )
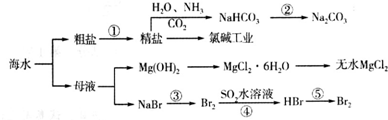

| A、要实现反应②可向NaHCO3溶液中加入过量石灰水 |
| B、溴元素在反应③、⑤中被氧化,在反应④中被还原 |
| C、工业上一般用金属钠与无水MgCl2反应制取Mg单质 |
| D、海水中含有碘元素,可将海水浓缩加热得到碘单质 |
一定条件下存在反应:2SO2(g)+O2 (g)═2SO3(g),其正反应放热.现有三个体积相同的密闭容器 I、Ⅱ、Ⅲ,按如图所示投料,并在400℃条件下开始反应.达到平衡时,下列说法正确的是( )


| A、容器I、Ⅲ中平衡常数相同 |
| B、容器Ⅱ、Ⅲ中正反应速率相同 |
| C、容器Ⅱ、Ⅲ中的反应达平衡时,SO3的体积分数:Ⅱ>Ⅲ |
| D、容器 I中SO2的转化率与容器 II中SO3的转化率之和小于1 |
下列五种有色溶液与SO2作用,均能褪色,其实质相同的是( )
①品红溶液 ②酸性KMnO4溶液 ③滴有酚酞的NaOH溶液 ④溴水 ⑤淀粉碘溶液.
①品红溶液 ②酸性KMnO4溶液 ③滴有酚酞的NaOH溶液 ④溴水 ⑤淀粉碘溶液.
| A、①④ | B、①②④ |
| C、②③⑤ | D、②④⑤ |
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、一定条件下,1.5 mol H2和0.5 mol N2充分反应后,可得到NH3的分子数为NA |
| B、常温常压下,18 g H2O中含有的电子总数为8NA |
| C、足量的Cu与Cl2反应生成0.2 mol产物时,失去的电子数为0.4NA |
| D、标准状况下,22.4 L己烯中含有的分子数为NA |
下列关于煤、石油、天然气等化石燃料的说法正确的是( )
| A、石油裂化得到的汽油是纯净物 |
| B、天然气是一种较为清洁的化石燃料 |
| C、石油产品都可用于聚合反应 |
| D、水煤气是指煤气中含有一定量的水 |
既能与NaOH溶液反应,又能与稀H2SO4溶液反应的物质是( )
| A、(NH4)2CO3 |
| B、Al(OH)3 |
| C、NaHSO4 |
| D、Na2SO3 |
 有如图所示的有机物,根据该有机物的结构回答:
有如图所示的有机物,根据该有机物的结构回答: 开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示:通入a气体的电极是原电池的
开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图所示:通入a气体的电极是原电池的