题目内容
17.下列正确的是( )| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH-═AlO2-+H2↑ | |
| C. | 用浓NaOH溶液溶解Al2O3:OH-+Al2O3═AlO2-+H2O | |
| D. | 可以用互滴法鉴别稀HCl溶液与NaAlO2溶液 |
分析 A.氨水为弱碱,反应生成氢氧化铝沉淀;
B.2molAl完全反应生成3mol氢气,该反应不满足电子守恒;
C.离子方程式中Al、H原子数不相等,违反了质量守恒;
D.盐酸不足时生成氢氧化铝沉淀,盐酸过量时生成氯化铝.
解答 解:A.氯化铝溶液中加入过量氨水,反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.浓烧碱溶液中加入铝片,反应生成偏铝酸钠和氢气,正确的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C.用浓NaOH溶液溶解Al2O3,反应生成偏铝酸钠和水,正确的离子方程式为:2OH-+Al2O3═2AlO2-+H2O,故C错误;
D.少量盐酸滴入NaAlO2溶液中,反应生成氢氧化铝沉淀,若少量NaAlO2滴入盐酸中,不会有沉淀生成,所以可用互滴法鉴别稀HCl溶液与NaAlO2溶液,故D正确;
故选D.
点评 本题考查了离子方程式的书写方法判断,为高考的高频题,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等;试题有利于培养学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.用玻璃棒蘸浓硫酸滴在纸上,纸变黑,这表现了浓硫酸的( )
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 |
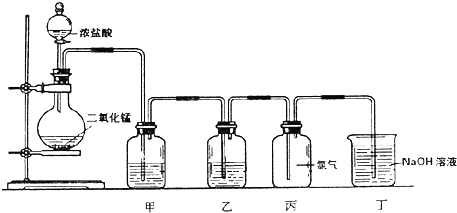
5.下列装置能达到实验目的是( )
| A. | 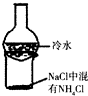 加热烧杯,可用来分离NaCl和NH4Cl | B. | 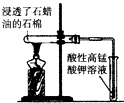 石蜡油分解实验 | ||
| C. |  比较MnO2、Cl2、S的氧化性 | D. | 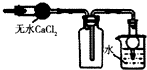 收集干燥的氨气 |
12.下列实验符合“绿色环保”思想的是( )
| A. |  制氯水 | B. |  铜与浓硫酸反应 | ||
| C. | 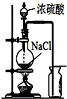 制氯化氢气体 | D. |  一氧化碳还原氧化铜 |
2.下列关于有机物的说法中,错误的是( )
| A. | 乙烯和甲烷都易发生取代反应 | |
| B. | 苯、乙醇和乙酸都能发生取代反应 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 用新制Cu(OH)2悬浊液可检验尿液中的葡萄糖 |
6.下列离子化合物的电子式书写不正确的是( )
| A. | 氯化钙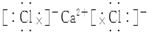 | B. | 硫化钠 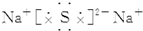 | C. | 氟化钾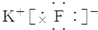 | D. | 过氧化钠 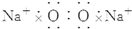 |
7.国际互联网上报道:目前世界上有近20亿人患有缺铁性贫血.这里的“铁”是指( )
| A. | 铁单质 | B. | +2价铁元素 | C. | +3价铁元素 | D. | 三氧化二铁 |