题目内容
10.多少克H2SO4所含的分子数与3.6克10%盐酸所含溶质的分子数相等?分析 3.6克10%盐酸所含溶质的分子的物质的量为:$\frac{3.6×10%}{36.5}$=0.01mol,即硫酸的物质的量为0.01mol,根据m=nM,进行计算求解.
解答 解:3.6克10%盐酸所含溶质的分子的物质的量为:$\frac{3.6×10%}{36.5}$=0.01mol,即硫酸的物质的量为0.01mol,m=nM=0.01mol×98g/mol=0.98g,答:0.98gH2SO4所含的分子数与3.6克10%盐酸所含溶质的分子数相等.
点评 本题主要考查有关化学式的计算中元素质量分数的计算、化合物质量的计算,难度稍大.

练习册系列答案
相关题目
18.下列物质的分类结果全部正确的是( )
| A. | SiO2酸性氧化物 Na2O碱性氧化物 A12O3两性氧化物 | |
| B. | 水玻璃-混合物 冰水混合物-纯净物 HT-单质 | |
| C. | 火碱-碱 石炭酸-羧酸 小苏打-酸式盐 | |
| D. | 王水-强电解质 硫酸钡-强电解质 醋酸-弱电解质 |
15.下列对物质用途的描述中,错误的是( )
| A. | 与Mg、Al比较,镁铝合金的强度和硬度均较大,常用作航天器的材料 | |
| B. | Cl2、SO2、NaClO均可用于漂白某些物质 | |
| C. | 浓硫酸具有吸水性,可用于干燥HCl、H2S、O2 | |
| D. | 碳酸钠可用于制皂和制玻璃 |
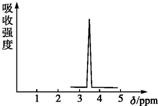 在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目.
在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目.
 zC(g)平衡时侧得A的浓度为0.50mol/L,保持温度不变,将容器的体积扩大两倍,测得A的浓度变为0.3mol/L,下列有关判断正确的是
zC(g)平衡时侧得A的浓度为0.50mol/L,保持温度不变,将容器的体积扩大两倍,测得A的浓度变为0.3mol/L,下列有关判断正确的是