题目内容
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂反应的△H (填“增大”“减小”或“不改变”).
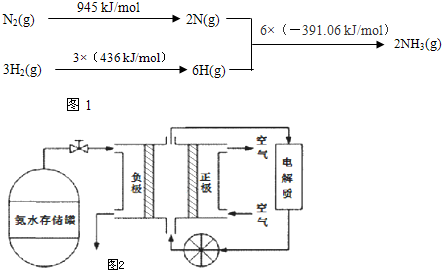
(2)O2 (g)=O+2(g)+e-△H1=+1175.7kJ?mol-1
PtF6(g)+e-1?PtF6-(g)△H2=-771.1kJ?mol-1
O2+PtF6-(s)=O2+(g)+PtF6-(g)△H3=+482.2kJ?mol-1
则反应O2(g)+PtF6(g)=O2+PtF6-(s)的△H= kJ?mol-1.
(3)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显 性(填“酸”“碱”或“中”);a 0.01(填“<”或“>”或“=”)
(1)合成氨反应反应N2(g)+3H2(g)?2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡
(2)O2 (g)=O+2(g)+e-△H1=+1175.7kJ?mol-1
PtF6(g)+e-1?PtF6-(g)△H2=-771.1kJ?mol-1
O2+PtF6-(s)=O2+(g)+PtF6-(g)△H3=+482.2kJ?mol-1
则反应O2(g)+PtF6(g)=O2+PtF6-(s)的△H=
(3)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显
考点:化学平衡的影响因素,用盖斯定律进行有关反应热的计算,酸碱混合时的定性判断及有关ph的计算
专题:
分析:(1)恒压条件下向平衡体系中通入氩气,体积增大,平衡向逆方向移动;催化剂对反应热不影响;
(2)根据盖斯定律可计算;
(3)根据溶液中阴阳离子的电荷相等判断溶液的酸碱性;
体积相等稀盐酸和氨水混合,若浓度相等,则恰好完全反应生成氯化铵,溶液显酸性,若溶液恰好呈中性时氨水应稍微过量,据此分析.
(2)根据盖斯定律可计算;
(3)根据溶液中阴阳离子的电荷相等判断溶液的酸碱性;
体积相等稀盐酸和氨水混合,若浓度相等,则恰好完全反应生成氯化铵,溶液显酸性,若溶液恰好呈中性时氨水应稍微过量,据此分析.
解答:
解:(1)恒压条件下向平衡体系中通入氩气,体积增大,平衡向逆方向移动;加入催化剂,只改变反应的活化能,但反应热不变;
故答案为:向左;不改变;
(2)①O2(g)=O2+(g)+e-△H1=+1175.7kJ?mol-1
②PtF6(g)+e-=PtF6-(g)△H2=-771.1kJ?mol-1
③O2PtF6(S)=O2+(g)+PtF6-(g)△H3=+482.2kJ?mol-1
据盖斯定律,①+②-③得:O2(g)+PtF6(g)=O2PtF6(s)△H=-77.6 kJ?mol-1,
故答案为:-77.6;
(3)根据溶液的电中性原则,c(NH4+)=c(Cl-),则c(H+)=c(OH-),则溶液显中性;
因体积、浓度相同的稀盐酸和氨水混合,溶液中的溶质为氯化铵,溶液呈酸性,若该溶液恰好呈中性,氨水应稍微过量,所以氨水的浓度大于盐酸的浓度.
故答案为:中;>.
故答案为:向左;不改变;
(2)①O2(g)=O2+(g)+e-△H1=+1175.7kJ?mol-1
②PtF6(g)+e-=PtF6-(g)△H2=-771.1kJ?mol-1
③O2PtF6(S)=O2+(g)+PtF6-(g)△H3=+482.2kJ?mol-1
据盖斯定律,①+②-③得:O2(g)+PtF6(g)=O2PtF6(s)△H=-77.6 kJ?mol-1,
故答案为:-77.6;
(3)根据溶液的电中性原则,c(NH4+)=c(Cl-),则c(H+)=c(OH-),则溶液显中性;
因体积、浓度相同的稀盐酸和氨水混合,溶液中的溶质为氯化铵,溶液呈酸性,若该溶液恰好呈中性,氨水应稍微过量,所以氨水的浓度大于盐酸的浓度.
故答案为:中;>.
点评:本题考查化学平衡移动的问题,侧重于化学平衡移动的综合考查和盖斯定律的应用,题目难度中等,学生只要掌握解答该题的关键,做题时注意体会.

练习册系列答案
相关题目
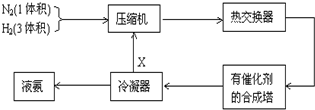 如图是合成氨的简要流程示意图,沿X路线回去的物质是( )
如图是合成氨的简要流程示意图,沿X路线回去的物质是( )| A、N2和H2 |
| B、催化剂 |
| C、NH3 |
| D、H2 |
在一定条件下,反应CO+NO2?CO2+NO 达到平衡后,降低温度,混合气体的颜色变浅.下列判断正确的是( )
| A、正反应为吸热反应 |
| B、正反应为放热反应 |
| C、CO的浓度增大 |
| D、各物质的浓度不变 |
下列实验可达到实验目的是( )
A、将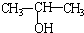 与NaOH的醇溶液共热制备CH3-CH═CH2 与NaOH的醇溶液共热制备CH3-CH═CH2 |
B、乙酰水杨酸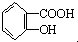 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备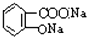 |
| C、向CH3CH2Br中滴入AgNO3溶液以检验溴元素 |
| D、甲苯在溴化铁催化作用下与液溴反应生成2,4,6-三溴甲苯 |
在一个体积恒定的密闭容器中,N2与H2反应合成氨的反应达到平衡后,容器中含 1molN2. 3molH2.1molNH3,保持温度不变,向该容器中再加1mol N2. 3mol H2.1molNH3,下列说法正确的是( )
| A、正.逆反应速率同时增大,平衡不移动 |
| B、正.逆反应速率同时增大,NH3百分含量增大 |
| C、正反应速率增大,逆反应速率减小,平衡向逆反应移动 |
| D、正.逆反应速率不变,平衡不移动 |
下列各组离子中,在溶液中能大量共存的是( )
| A、HCO3-、Cl-、Na+、H+ |
| B、Al3+、K+、OH-、SO42- |
| C、Fe2+、NO3-、SO42-、H+ |
| D、K+、Al3+、SO42-、NO3- |
下列事实中,不能用勒夏特列原理解释的是( )
| A、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B、由H2(g)、I2(g)、HI(g)组成的平衡体系,压缩容器体积后颜色加深 |
| C、实验室中常用排饱和食盐水的方法收集氯气 |
| D、工业上生产硫酸的过程中使用适当过量的空气以提高二氧化硫的利用率 |
2.8gFe全部溶于一定浓度、200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断正确的是( )
| A、反应后溶液中存在Fe3+和Fe2+ |
| B、1.12L气体是NO、NO2的混合气体 |
| C、反应后溶液中c(NO3-)=0.85mol?L-1 |
| D、反应后的溶液最多还能溶解1.4gFe |