题目内容
如果1g水中含有n个氢原子,则阿伏加德罗常数的值为( )
| A、18n | B、9n |
| C、2n | D、n/9 |
考点:物质的量的相关计算
专题:计算题
分析:根据水分子的构成、n=
、N=n×NA来计算.
| m |
| M |
解答:
解:1g水的物质的量=
=
mol,水分子是由1个氧原子和2个氢原子构成的,则氢原子的物质的量为
mol×2=
mol,
由N=n×NA可知,阿伏加德罗常数可表示为NA=
=9nmol-1,
故选B.
| 1g |
| 18g/mol |
| 1 |
| 18 |
| 1 |
| 18 |
| 1 |
| 9 |
由N=n×NA可知,阿伏加德罗常数可表示为NA=
| n | ||
|
故选B.
点评:本题考查阿伏伽德罗常数的计算,明确质量、物质的量、微粒数目的关系是解答本题的关键,并注意不同字母表示的意义来解答

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
在实验室中,通常将金属钠保存在( )
| A、水中 | B、四氯化碳中 |
| C、煤油中 | D、酒精中 |
下列电离方程式中正确的是( )
| A、Na2CO3=Na2++CO32- |
| B、FeCl3=Fe2++3Cl- |
| C、H2SO4=H2++SO42- |
| D、NH4NO3=NH4++NO3- |
最近媒体报道了一些化学物质,如:爆炸力极强的N5、结构类似白磷的N4、比黄金还贵的18O2、太空中的甲醇气团等.下列说法正确的是( )
| A、18O2和16O2是两种不同的核素 |
| B、将a克铜丝灼烧成黑色后趁热插入甲醇中,铜丝变红,质量小于a克 |
| C、N4分子为正方形结构,每个分子中含有6个共价键 |
| D、一定条件下2N5=5N2是化学变化 |
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去).关于混合粉末的组成判断正确的是( )


| A、一定含CuO和C |
| B、一定含Fe2O3、CuO和C |
| C、一定含CuO和C,一定不含Al |
| D、气体Z为纯净物 |
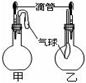 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响).则所用试剂分别可能依次是( )| A、甲:铝粉和浓NaOH溶液 乙:饱和NaCl溶液和Cl2 |
| B、甲:双氧水和MnO2 乙:NaOH溶液和CO2 |
| C、甲:浓氨水和碱石灰 乙:浓氨水和SO2 |
| D、甲:水和CO2 乙:水和氯化氢 |
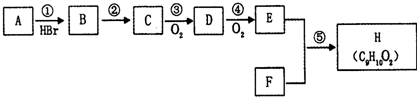
 A、C、D、E、F五种有机物可发生如图所示的转化.已知:C的结构简式为
A、C、D、E、F五种有机物可发生如图所示的转化.已知:C的结构简式为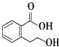 ,D能跟NaHCO3发生反应,D和E的相对分子质量相等,F为无支链的化合物.
,D能跟NaHCO3发生反应,D和E的相对分子质量相等,F为无支链的化合物.