题目内容
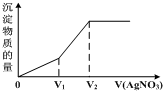 往含有S2-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中c(S2-)和c(Cl-)的比值为( )
往含有S2-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中c(S2-)和c(Cl-)的比值为( )A、
| ||
B、
| ||
C、
| ||
D、
|
分析:先根据图象中测定物质的量与硝酸根体积关系判断0-V1、V1-V2生成沉淀离子,然后根据反应方程式计算出原溶液中c(S2-)和c(Cl-)的比值.
解答:解:溶液中的反应为S2-+2Ag+=Ag2S↓,Cl-+Ag+=AgCl↓,由图象可知,先生成硫化银沉淀后生成氯化银沉淀,加入V1体积硝酸银,硫离子沉淀完全,则n(S2-)=
c(AgNO3)×V1,加入V2体积的硝酸银,氯离子沉淀完全,则n(Cl-)=c(AgNO3)×(V2-V1),体积相同,浓度之比等于物质的量之比,所以原溶液中原溶液中
=
=
,
故选D.
| 1 |
| 2 |
| c(S2-) |
| c(Cl-) |
| ||
| c(AgNO3)×(V2-V1) |
| V1 |
| 2(V2-V1) |
故选D.
点评:本题考查了难溶电解质的溶解平衡以及沉淀转化的知识,题目难度不大,可以根据教材知识来回答,试题培养了学生分析、良好能力及灵活应用所学知识能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
往含有S2-和Cl-的稀溶液中逐滴加入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。则原溶液中c(S2-)/c(Cl-)的比值为:
| A.2V1/V2 | B.2(V2-V1)/V1 | C.2V2/V1 | D.V1/2(V2-V1) |
 往含有S2-和Cl-的稀溶液中逐滴加入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中
往含有S2-和Cl-的稀溶液中逐滴加入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中
 的比值为( )
的比值为( )



