题目内容
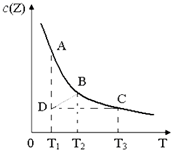 已知在一密闭容器中存在如下化学平衡:X(g)+3Y(g)?2Z(g),其中c(Z)与温度(T)的关系如图所示(曲线上任何一点都表示平衡状态).下列说法中正确的是( )
已知在一密闭容器中存在如下化学平衡:X(g)+3Y(g)?2Z(g),其中c(Z)与温度(T)的关系如图所示(曲线上任何一点都表示平衡状态).下列说法中正确的是( )| A、B点对应的反应速率大于C点对应的反应速率 |
| B、状态A的c(Y)大于状态D c(Y) |
| C、反应X(g)+3Y(g)?2Z(g)的△H<0 |
| D、其他条件不变,缩小容器的体积,平衡可由D点移动到B点 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:该反应是气体体积减小的反应,Z的浓度随温度的升高而减小,说明正反应放热,据此分析.
解答:
解:A、C点温度比B点高,C点反应速率比B点快,故A错误;
B、状态A的c(Z)大于状态D c(Z),所以状态A的c(Y)小于状态D c(Y),故B错误;
C、Z的浓度随温度的升高而减小,说明正反应放热,故C正确;
D、其他条件不变,缩小容器的体积,则温度相同,而D、B两点的温度不同,故D错误;
故选C.
B、状态A的c(Z)大于状态D c(Z),所以状态A的c(Y)小于状态D c(Y),故B错误;
C、Z的浓度随温度的升高而减小,说明正反应放热,故C正确;
D、其他条件不变,缩小容器的体积,则温度相同,而D、B两点的温度不同,故D错误;
故选C.
点评:本题考查了据温度浓度图象判断反应速率和浓度的变化以及平衡状态的判断,题目难度中等.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
在一定温度下,一定体积的密闭容器中有如下平衡:H2(气)+I2(气)?2HI(气)
已知H2和I2的起始浓度均为0.01mol?L-1时,达平衡时HI的浓度为0.16mol?L-1.若H2和I2的起始浓度均变为0.20mol?L-1,则平衡时H2的浓度(mol?L-1)是( )
已知H2和I2的起始浓度均为0.01mol?L-1时,达平衡时HI的浓度为0.16mol?L-1.若H2和I2的起始浓度均变为0.20mol?L-1,则平衡时H2的浓度(mol?L-1)是( )
| A、0.16 | B、0.08 |
| C、0.04 | D、0.02 |
下列有关金属冶炼的说法中错误的是( )
| A、炼铁中加入焦炭作造渣剂 |
| B、炼钢中吹入氧气作氧化剂 |
| C、电解铝生产中加入冰晶石以降低氧化铝的熔点 |
| D、火法冶金比湿法冶金能耗大 |
下列物质的水溶液pH最大的是( )
| A、NaHCO3 |
| B、KHSO4 |
| C、AlCl3 |
| D、CH3COONa |
关于钠及其化合物性质的叙述,不正确的是( )
| A、过氧化钠是淡黄色固体,可用于呼吸面具中作为氧气的来源 |
| B、氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 |
| C、碳酸钠固体中混有少量碳酸氢钠,可用加热的方法除去 |
| D、质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体多 |
据报道,最近某公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.则下列说法正确的是( )
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、充电时有CH3OH生成的电极为阴极 |
| C、放电时电解质溶液的pH逐渐增大 |
| D、充电时每生成1 mol CH3OH转移12 mol电子 |
下列溶液中Cl-的物质的量浓度与l00mL1moL/LMgCl2溶液中Cl-的物质的量浓度相同的是( )
| A、50mL2mol/LCaCl2溶液 |
| B、100mL2moL/LNaCl溶液 |
| C、50mL4mol/LCaCl2溶液 |
| D、100mL4mol/LNaCl溶液 |

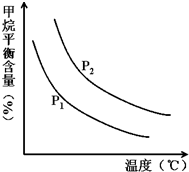 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下: