题目内容
3.将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,此液体不具有的性质是( )| A. | 光束通过该液体时形成光亮的“通路” | |
| B. | 插入石墨电极通直流电后,有一极附近液体颜色加深 | |
| C. | 向该液体中加入硝酸银溶液,无沉淀产生 | |
| D. | 向该液体中逐滴滴入过量的稀硫酸,会看到液体先生成红褐色沉淀,后沉淀溶解 |
分析 将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体即制得氢氧化铁胶体,根据胶体中分散质粒子直径在1-100nm之间,胶体能发生丁达尔效应、能产生电泳现象、能产生聚沉分析.
解答 解:将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体即制得氢氧化铁胶体,
A、胶体中分散质粒子直径在1-100nm之间,所以胶体能产生丁达尔效应,则光束通过该液体时形成光亮的“通路”,故A正确;
B、胶体具有吸附性,吸附带电荷的离子,所以能产生电泳现象,则插入石墨电极通直流电后,氢氧化铁胶粒移向某一极,液体颜色加深,故B正确;
C、饱和FeCl3溶液中能电离出氯离子,加入硝酸银溶液可生成沉淀,故C错误;
D、向该液体中逐滴滴入过量的稀硫酸,先产生聚沉,生成氢氧化铁沉淀,后硫酸溶解氢氧化铁沉淀,所以会看到液体先生成红褐色沉淀,后沉淀溶解,故D正确;
故选:C.
点评 本题考查了胶体的性质,难度不大,注意胶体与其他分散系的本质区别是:胶体粒子的直径在1-100nm之间.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
13.化学知识在生产和生活中有着重要的应用.下列说法中不正确的是( )
| A. | 铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 | |
| B. | 发酵粉中含有的碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| C. | Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦杆、羽毛等 | |
| D. | 明矾能水解生成Al(OH)3胶体,常用作生活用水的消毒剂 |
14.有同学研究从矿石开始到产出钢铁的工艺流程.
(1)将6.62g铁矿石样品投入足量的盐酸中完全溶解后过滤,滤渣中不含铁元素.在滤液中加过量的NaOH溶液,充分反应,过滤、洗涤、灼烧得4.80g Fe2O3,求该铁矿石含铁的质量分数.
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00吨生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(3)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况).计算此钢样粉末中铁和碳的物质的量之比.
(4)再取三份不同质量的上述钢样粉末,分别加到100mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
计算硫酸溶液的物质的量浓度
(5)若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
(1)将6.62g铁矿石样品投入足量的盐酸中完全溶解后过滤,滤渣中不含铁元素.在滤液中加过量的NaOH溶液,充分反应,过滤、洗涤、灼烧得4.80g Fe2O3,求该铁矿石含铁的质量分数.
(2)现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00吨生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(3)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况).计算此钢样粉末中铁和碳的物质的量之比.
(4)再取三份不同质量的上述钢样粉末,分别加到100mL相同浓度的H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
(5)若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
18.在 KNO3+S+C→K2S+N2+CO2反应中,被1mol KNO3氧化的碳的质量是( )
| A. | 21g | B. | 18g | C. | 15g | D. | 12g |
8.某有机物的结构简式如图所示,有关该有机物的叙述不正确的是( )
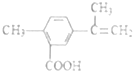

| A. | 在一定条件下,能发生取代、氧化、酯化和加聚反应 | |
| B. | 该物质分子中最多可以有11个碳原子在同一平面上 | |
| C. | 1mol该物质最多可与4molH2发生加成反应 | |
| D. | 1mol该物质完全氧化最多可消耗14mol氧气 |
15.在一可变容积的密闭容器中进行反应:C(s)+H2O(g)?CO(g)+H2(g),下列条件的改变对反应速率几乎无影响的是( )
| A. | 增加H2O(g) 的量 | |
| B. | 增加C(s)的量 | |
| C. | 将容器的体积缩小一半 | |
| D. | 保持压强不变,充入N2,使容器的体积变大 |
12.下列说法错误的是( )
| A. | 用铁制容器盛放硫酸铜溶液,容器易被腐蚀 | |
| B. | 利用催化措施,可以将汽车尾气中的CO和NO转化为无害气体 | |
| C. | 防止酸雨发生的重要措施之一是使用清洁能源 | |
| D. | 氧化铜呈红色,可作为制造陶瓷的红色颜料 |
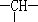 和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体)( )
和一个-Cl,它的可能的结构有几种(本题不考虑对映异构体)( )